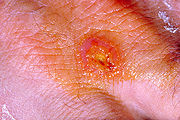
- Parinaud-Krankheit
-
Klassifikation nach ICD-10 A21.- Tularämie A21.0 Ulzeroglanduläre Tularämie A21.1 Okuloglanduläre Tularämie A21.2 Pulmonale Tularämie A21.3 Gastrointestinale Tularämie Abdominale Tularämie
A21.7 Generalisierte Tularämie A21.8 Sonstige Formen der Tularämie A21.9 Tularämie, nicht näher bezeichnet ICD-10 online (WHO-Version 2006) Tularämie ist eine tödlich verlaufende ansteckende Erkrankung bei frei lebenden Nagetieren, die durch das Bakterium Francisella tularensis ausgelöst wird. Die Erkrankung kann auf den Menschen übertragen werden.
Da das Beschwerdebild dem der Pest ähnelt und die Erkrankung sehr häufig Hasen und Wildkaninchen befällt, wird sie häufig auch als Hasenpest bezeichnet. Andere Namen sind Nagerpest, Lemmingfieber, Parinaudkrankheit und Hirschfliegenfieber.
Inhaltsverzeichnis
Geschichte
Erstmals wurde die Erkrankung 1911 durch den Mediziner George W. McCoy beschrieben. 1912 gelang Charles W. Chapin die Isolierung des Erregers aus einer Eichhörnchenart in Kalifornien. Zwischen 1919 und 1928 beschäftigte sich Edward Francis sehr ausführlich mit der Erkrankung und benannte sie nach dem Ort Tulare in Kalifornien/USA. Der wissenschaftliche Name des Erregers wurde ebenfalls nach ihm benannt. In Europa wurde die Tularämie zum ersten Mal 1931 dokumentiert, und zwar an der Ostseeküste Mittelschwedens. Zwischen 1936 und 1950 gelang den sowjetischen Wissenschaftlern H. A. Gaiski, B. Y. Elbert, Somov und Chatenever die Entwicklung eines Impfstoffes gegen die Tularämie.
Während des Zweiten Weltkrieges wurden an der osteuropäischen Front Epidemien mit mehr als Hunderttausend Infektionen gemeldet. Der ehemalige sowjetische Biowaffenforscher Ken Alibek vermutet, dass die Epidemien die Folge eines Einsatzes von Francisella tularensis als biologische Waffe waren.[1]
In den 1950er und 1960er Jahren entwickelte das US-Militär Waffensysteme, die das Bakterium als Aerosol verteilen sollten. 1969 schätzte ein Expertengremium der Weltgesundheitsorganisation, dass eine derartige Verteilung von 50 Kilogramm F. tularensis über einer Stadt mit 5 Millionen Einwohnern in 250.000 Kampfunfähigen und 19.000 Toten resultieren würde.[1] 1997 schätzten Wissenschaftler der amerikanischen CDC die Folgekosten eines solchen, terroristischen Angriffs auf 5,4 Milliarden US-Dollar pro 100.000 dem Agens ausgesetzten Personen.[2]
Der größte dokumentierte Tularämie-Ausbruch fand 1966–1967 in einem Farmgebiet Schwedens statt und betraf etwa 600 Patienten. Diese hatten sich überwiegend beim Umschichten infizierten Heus durch Inhalation mit dem milderen Typ B infiziert und sprachen gut auf Tetrazyklin an, sodass keine Todesfälle verzeichnet wurden.[1]
Erreger
Der Erreger der Tularämie ist das hochansteckende Bakterium Francisella tularensis (früher auch: Pasteurella tularensis). Es handelt sich um ein sehr kleines, gramnegatives, kokkoides, sporenloses, schwer anzüchtbares Stäbchen, das den γ-Proteobakterien (Familie Pasteurellaceae) zugeordnet wird. Das Bakterium wird durch Wärme und die herkömmlichen Desinfektionsmittel zerstört, ist aber gegenüber Kälte resistent. Bereits 10 bis 50 Bakterien als Aerosol können einen Menschen infizieren. Der Erreger kann in gefrorenem Hasenfleisch bis zu 3 Jahre und in Boden und Wasser über mehrere Wochen überdauern.
Es sind zwei Varianten bekannt:
- Francisella tularensis biovar tularensis (Typ A) in Nordamerika, der für gefährlichere Verläufe verantwortlich ist.
- Francisella tularensis biovar palaearctica (Typ B) mit weltweiter Verbreitung.
Als Reservoirwirte dienen vor allem Tiere wie Hasen, Biber und Schildzecken.
Verbreitung
- Nordamerika zwischen 30°N und 71°N: USA (vor allem Arkansas, Missouri, Oklahoma, Tennessee, Kansas und Utah, andere Bundesstaaten außer Hawaii), Kanada und Mexiko – 1.500 Infektionen pro Jahr
- Ostasien mit Japan (1.400 Infektionen in 70 Jahren) und Westrussland
- Europa: insbesondere Skandinavien (20–50 pro Jahr), Tschechien (10), Slowakei (10), Spanien (55 Fälle seit 1997), Serbien (weitgehend in Kosovo und Metochien, 2001 bis März 2002 700 Fälle), Deutschland (2003 und 2004 jeweils drei Fälle, 2005 zehn).
Im Oktober 2005 infizierten sich bei einer Treibjagd auf Hasen im Landkreis Darmstadt-Dieburg neun Jäger und Treiber mit Tularämie. Fast alle waren am Ausnehmen oder Abbalgen beteiligt, sie hatten keine Krankheitszeichen an den Tieren festgestellt. Bei einem weiteren Jäger, der etwa vier Wochen später verstarb, wurde die Krankheit als Todesursache angenommen, da er typische Symptome gezeigt hatte.
Kurz nach dem Zweiten Weltkrieg war die Krankheit in Deutschland wesentlich häufiger, vermutlich aufgrund der damals höheren Hasen- und Kaninchenpopulation und der stärkeren Nutzung dieser Tiere für die menschliche Ernährung. Rund 100 bis 200 Fälle wurden in dieser Zeit pro Jahr registriert.
Nach dem deutschen Infektionsschutzgesetz besteht eine Meldepflicht der Erkrankung. Nach dem deutschen Tierseuchengesetz bzw. der Verordnung über meldepflichtige Tierkrankheiten ist der Nachweis von F. tularensis bei Tieren ebenfalls meldepflichtig
Infektionsweg
Als Vektoren für den Erreger sind blutsaugende Ektoparasiten festgestellt, also auf der Körperoberfläche lebende Parasiten, wie z. B. Mücken, Flöhe, Läuse, Wanzen, Milben oder Zecken. Die Parasiten kommen auf wild lebenden Nagetieren wie (Hasen, Wildkaninchen, Ratten, Mäuse, Eichhörnchen) vor, seltener auf Wildgeflügel, Fuchs, oder Nutz- und Haustieren (Schafe, Schweine, Rinder, Hunde, Katzen, Hamster).
Übertragung:
- über direkten und indirekten Kontakt mit infektiösen Nagetieren (auch: Jagen, Enthäuten oder Schlachten)
- indirekt über die genannten blutsaugenden Ektoparasiten als Vektoren
- über Schlamm oder verunreinigtes Wasser
- durch das Einatmen erregerhaltigen Staubes (verunreinigtes Heu, Silofutter, Erde, Staub), wobei nur wenige Bakterien bereits zu einer Erkrankung führen
- durch Verzehr von ungenügend erhitztem erregerhaltigem Fleisch.
Übertragungen von Mensch zu Mensch sind nicht bekannt geworden (sogenannte Anthropozoonose).
Inkubationszeit
Die Inkubationszeit der Tularämie bei Tieren beträgt zwei bis drei Tage. Beim Menschen liegt sie bei zwei bis zehn Tagen, kann aber auch bis zu 30 Tagen betragen.
Krankheitsverlauf und Symptome
Die Tularämie verläuft bei Tieren und beim Menschen unterschiedlich.
Tularämie bei Tieren
Nach Übertragung der Erreger durch Parasiten auf die Nagetiere kommt es nach zwei bis drei Tagen zu einer Septikämie, also einer Aussaat der Erreger mit dem Blut. Die Tiere fallen durch Schwäche, Fieber, eine gesteigerte Atmungsfrequenz und fehlendes Fluchtverhalten auf. Lymphknoten und Milz sind vergrößert. Innerhalb von vier bis dreizehn Tagen sind die meisten Tiere verstorben. Chronisch verlaufende Infektionen enden nach 14 bis 60 Tagen tödlich.
Tularämie beim Menschen
Äußere (lokalisierte) Formen
- ulzeroglanduläre (kutanoglanduläre) Tularämie - Häufigste Form der Tularämie (75–85 %), die mit plötzlichem Fieberanstieg beginnt. Es bilden sich Geschwüre an der Eintrittsstelle mit regionaler, oft eitriger, Entzündung der Lymphknoten.
- okuloglanduläre Tularämie (Parinaudkonjunktivitis) - Die Eintrittspforte an der Bindehaut des Auges ist durch ein gelbliches Knötchen erkennbar, die Lymphknoten vor dem Ohr und im Hals sind geschwollen. Zusätzlich kommt es zu einer sehr schmerzhaften Konjunktivitis.
- glanduläre Tularämie - Es ist keine Eintrittspforte erkennbar und die Bildung von Geschwüren fehlt.
- glandulo-pharyngeale Tularämie - Diese Form ist vor allem bei Kindern zu erkennen. Es sind Geschwüre in der Mundhöhle und im Rachen zu erkennen, die Lymphknoten im Kiefernwinkel sind geschwollen.
Innere (invasive) Formen
Die innere Form der Tularämie entsteht, wenn die Erreger eingeatmet werden oder auf dem Blutweg innere Organe erreichen. Es handelt sich dann um eine hochfieberhafte, gefährliche Erkrankung mit einer deutlich höheren Letalität als bei den äußeren Formen.
- typhöse (generalisierte oder septische) Tularämie - Diese Form entsteht vor allem bei Laborinfektionen oder nach dem Kontakt mit infizierten Schlachtblut: sehr oft sind die Lungen befallen, die Patienten haben immer Fieber, Kopfschmerzen und Schweißausbrüche; Komplikationen sind Lungenabszesse, Mediastinitis, Meningitis, Perikarditis, Osteomyelitis, Rhabdomyolyse.
- intestinale Tularämie - Übertragung wahrscheinlich durch den Verzehr ungenügend erhitzten Fleisches infizierter Tiere. Symptome sind Pharyngitis, Übelkeit, Erbrechen, Durchfälle und abdominelle Schmerzen.
- thorakale (pulmonale) Tularämie - Am zweithäufigsten. Betrifft bevorzugt die Lunge und äußert sich dann als Pneumonie, also Lungenentzündung. Die Patienten leiden unter Husten, Auswurf, Luftnot und Schmerzen im Brustkorb.
- abdominelle Tularämie - Typhusähnliches Krankheitsbild, bei dem Leber und Milz geschwollen sind, die Patienten klagen über Bauchschmerzen und Durchfall.
Diagnose
Die Diagnose der Erkrankung wird im Tierversuch gestellt. Dazu wird erregerhaltiges Material auf Meerschweinchen, Ratten oder Mäuse übertragen. Indirekter Erregernachweis serologisch mit Agglutinationstest gegen Ende der 2. Woche. Der serologische Erregernachweis ist schwierig, da Kreuzreaktionen, z. B. mit dem Erreger von Typhus möglich sind.
Therapie
Die Behandlung besteht in der Gabe von Antibiotika. Am wirksamsten ist Streptomycin. Alternativ kann Doxycyclin oder Gentamicin eingesetzt werden. Die Erreger sind aber auch empfindlich gegenüber Tetrazyklinen, Erythromycin und Chloramphenicol. Gegenüber Penicillin und Sulfonamiden besteht jedoch eine Resistenz.
Prognose
Bei der inneren Form der Tularämie des Menschen handelt sich um eine schwere, lebensbedrohliche Erkrankung, die behandelt in ca. 5 % der Fälle tödlich verläuft. Ohne antibiotische Behandlung kann die Sterblichkeit über 30 % betragen.
Die amerikanischen Tularämieformen haben eine höhere Virulenz, mit einer Letalität von 10 bis 35 %, als die europäischen Stämme. Hier liegt die Letalität bei ungefähr 5 %.
Prophylaxe
Es existiert ein attenuierter Lebendimpfstoff (USA, GUS), er ist in Deutschland aber derzeit nicht verfügbar.
Eine medikamentöse Prophylaxe nach wahrscheinlicher Exposition (z. B. im Labor): Doxycyclin oder Ciprofloxacin für 14 Tage sollte rasch (möglichst innerhalb von 24 Stunden nach Exposition) begonnen werden. Falls eine mögliche Exposition erst nach Auftreten von Krankheitsfällen in Betracht gezogen wird, sollten alle mutmaßlich Exponierten ein Fieber-Monitoring für 21 Tage (nach der vermuteten Exposition) durchführen. Diejenigen, die in diesem Zeitraum eine grippeähnliche Erkrankung oder Fieber entwickeln, sollten therapiert werden, wie oben beschrieben. Das Überstehen der Erkrankung hinterlässt eine langjährige Immunität.
Quellen
- ↑ a b c D.T. Dennis et al.: „Tularemia as a Biological Weapon“. In: Journal of the American Medical Association. 21, Nr. 285, 2001, S. 2763-2773. PMID 11386933
- ↑ AF Kaufmann, MI Meltzer, GP Schmid: „The Economic Impact of a Bioterrorist Attack: Are Prevention and Postattack Intervention Programs Justifiable?“. In: Emerging Infectious Diseases. 3, Nr. 2, 1997. URL
Literatur
- H. Krauss, A. Weber, M. Appel, B. Enders, A. v. Graevenitz, H. D. Isenberg, H. G. Schiefer, W. Slenczka, H. Zahner: Zoonosen. Von Tier zu Mensch übertragbare Infektionskrankheiten. 3. vollständig überarbeitete und erweiterte Auflage, 605 Seiten. Deutscher Ärzte-Verlag, Köln, 2004. ISBN 3-7691-0406-4
- H. Krauss, A. Weber, M. Appel, B. Enders, A. v. Graevenitz, H. D. Isenberg, H. G. Schiefer, W. Slenczka, H. Zahner: Zoonoses. Infectious Diseases Transmissible from Animals to Humans. 3rd Edition, 456 pages. ASM Press. American Society for Microbiology, Washington DC., USA. 2003. ISBN 1-55581-236-8
- H. Krauss, A. Weber, B. Enders, H. G. Schiefer, W. Slenczka,H. Zahner: Zoonosen [Arabisch]. 688 Seiten. ACATAP, Damaskus, Syrien. 2001.
Weblinks
- Tularämie – Informationen des Robert Koch-Instituts
- Beschreibung bei der deutschen Gesellschaft für Reise- und Touristikmedizin
- Epidemiologisches Bulletin 16. Dezember 2005 / Nr. 50
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.