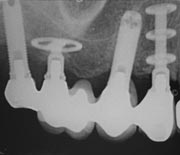
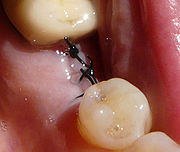
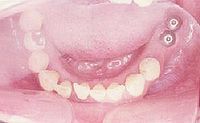
- Basale Implantate
-
Ein Zahnimplantat (von lat. in „im, hinein“ und planta „Steckling, Setzling“)[1] ist ein in den Kieferknochen eingesetzter Fremdkörper (Implantat). Das Teilgebiet der Zahnheilkunde, das sich mit der Insertion (Einsetzen) von Zahnimplantaten in den Kieferknochen befasst, wird als Implantologie bezeichnet. Durch ihre Verwendbarkeit als Träger von Zahnersatz übernehmen Zahnimplantate die Funktion künstlicher Zahnwurzeln. Hierbei werden sie im Allgemeinen (über ihr Schraubgewinde) in den Kieferknochen (enossale Implantate) eingedreht oder einfach eingesteckt. Sie verbinden sich innerhalb von 3 bis 6 Monaten mit dem umgebenden Knochen zu einer festen, äußerst belastungsfähigen Trägereinheit (Osseointegration).
Die makromorphologische Gestaltung des Implantates (Implantatform) hat Auswirkungen auf die chirurgische Insertionstechnik. Die Gestalt des aus dem Kieferknochen herausragenden Pfeilers bestimmt die Möglichkeiten der Suprakonstruktion. Unter Suprakonstruktion ist in diesem Zusammenhang der auf den Implantaten einzugliedernde Zahnersatz zu verstehen. Zahnimplantate bestehen üblicherweise aus Titan, aber auch aus keramischen Materialien.
Implantatsysteme und -formen
Nach langen Jahrzehnten mit verschiedenen, heute zum Teil naiv anmutenden Implantatformen aus der Vorkriegszeit, haben sich heute die sogenannten rotationssymmetrischen Implantate (meist Schraubenimplantate) durchgesetzt.
Das bedeutet, dass der Implantatkörper im Querschnitt kreisrund ist, so dass der Hohlraum, der das Implantat aufnehmen soll, mit rotierenden Instrumenten, z. B. einem Kanonenbohrer, in den Kieferknochen präpariert werden kann.
Dieses chirurgische Vorgehen ist vergleichsweise einfach und schnell, belastet den Patienten weniger als andere Implantationstechniken und führt nur sehr selten zu Komplikationen bei der Wund- und Einheilung. Zudem haben Schraubenimplantate den Vorteil, dass sie sich durch ihr Gewinde sofort im Knochen „festsetzen“ (primäre Stabilität). Das verkürzt die Einheilzeit, weil nur wenig Knochen „nachwachsen“ muss. Zunehmend werden die zylindrische Grundformen am Ende verjüngt, so dass insgesamt eine gestreckte Kegelform entsteht.
Am meisten haben sich mehrteilige Zahnimplantate durchgesetzt, weil sie durch ihre Kombinationsmöglichkeit den vorgegebenen Verhältnissen am Besten gerecht werden und gewährleistet ist, dass das Implantat während der Einheilphase nicht belastet wird. Mehrteilige Implantate bestehen aus dem im Knochen verankerten Körper, dem im Bereich der Mundschleimhaut liegenden Halsteil und dem Kopfteil, das die Suprakonstruktion aufnimmt. Die drei Teile werden miteinander verschraubt
Bei einteiligen Zahnimplantaten ragt der Implantatkopf unmittelbar nach der Insertion aus der Schleimhaut heraus. Somit ist es schwieriger, eine Belastung während der Einheilphase zu vermeiden.
Zirkon-Implantate sind immer einteilig, weil sie nicht so fein gefertigt werden können, um sie mehrteilig zu konzipieren.
Neben diesen zylinderförmigen Implantaten mit oder ohne Schraubgewinde gibt es auch flache, blattförmige Implantate (Extensionsimplantate), die entlang des Knochenverlaufes der Kiefer in einen ca. 1 mm breiten dort hineinpräparierten Schlitz von 4 bis 14 mm Länge eingesenkt werden und dort festwachsen. Diese Implantate haben zusätzlich Durchbohrungen, durch die der Knochen auch horizontal hindurchwachsen kann.
Eine weitere Gruppe bilden die Diskimplantate. Diese gehören zur Gruppe der BASAL-Implantate. Diskimplantate haben die Form eines skelettierten Zylinders und werden seitlich in den Kiefer eingesetzt. Der Halt erfolgt in der harten und gut durchbluteten Außenwand des Knochens. Diskimplantate können unter Umständen sofort belastet werden. Wegen ihrer besonderen Form sollen sie auch bei geringer Knochenhöhe bzw. fortgeschrittenem Knochenschwund eine stabile Einheilung gewährleisten.
Weltweit gibt es etwa 80 größere Hersteller und über 200-300 unterschiedliche Implantatformen. Die Schraubenimplantate unterscheiden sich vor allem in ihrer Konizität und der Art des Gewindes.
Historisch gesehen gab es außer den aktuellen schrauben- oder wurzelförmigen und zylindrischen Implantaten noch diverse andere Formen und Typen. Die meisten dieser Formen haben sich aber in der Praxis nicht bewährt.
Dies gilt insbesondere für die subperiostalen Implantate, die möglichst großflächig unter der Schleimhaut direkt dem Knochen aufliegen. Sie wurden vor allem bei hochgradigem Knochenschwund eingesetzt, wenn der Kieferknochen für Zylinder- oder Extensionsimplantate zu flach oder zu schmal war. Die bloße Auflagerung des flachen subperiostalen Implantates unter die Knochenhaut (Periost) führte oft zu großflächigen Entzündungen mit z. T. erheblichen ausgedehnten Knocheneinschmelzungen, weil ein wirksamer Infektionsschutz durch einen bakteriendichten Abschluss fehlt, wie er bei enossalen Implantaten gegeben ist.
Obwohl es in den USA große Erfolge bei subperiostalen Implantaten gibt (über 95% nach fünfjähriger Verweildauer bei einseitigen Unterkieferimplantaten)[2] , ist deren wissenschaftliche Entwicklung in Deutschland nicht weiter vorangetrieben worden. Der Grund liegt im wesentlichen darin, dass die Erkenntnisse der Knochenbiologie im Hinblick auf die zuverlässige Regeneration des Knochengewebes Möglichkeiten eröffnen, durch geeignete chirurgische Maßnahmen auch in Fällen eines knappen Knochenangebotes, Zylinderimplantate einzusetzen. Es gibt in Deutschland somit auch keinen Hersteller für subperiostale Gerüstimplantate.
Die früher verwendeten reinen Keramik-Implantate zeichneten sich durch ein hervorragendes Einwachsen aus. Jedoch traten sehr häufig Brüche auf, da die Keramik spröde (höheres Elastizitätsmodul) ist und Alterungsprozessen unterliegt. Knochen ermöglicht als biologisches Gewebe mehr oder weniger ausgeprägte Biegungen, die Keramiken nicht mitmachen. Daher hat man diese Materialgruppe weitgehend verlassen.
Implantatmaterial
Zahnärztliche Implantologie ist verhältnismäßig alt, gilt aber unter evidenzbasierten Gesichtspunkten auch heute noch als medizinisches Neuland. Schon vor 2000 bis 3000 Jahren wurden unterschiedliche Materialien für den Ersatz eines Zahnes im Kieferknochen benutzt. Es gibt Schädelfunde, bei denen Reihen von aus Quarz geschnitzten Zähnen gefunden wurden. Zahlreiche andere organische und anorganische Materialien wurden verwendet. Elfenbein und Holz, unterschiedliche Metalle, auch Eisen und neuerdings Kunststoffe wurden als Implantate schon eingesetzt. Unter allen Fremdkörpern hat sich Titan in den letzten 20 bis 30 Jahren am überzeugendsten durchgesetzt. Die Verbindung zwischen der Titanoberfläche und dem Knochen ist unter normalen, infektionsfreien Umständen in vielerlei Hinsicht am zuverlässigsten. Auch kommt es nur sehr selten zu Frakturen des Implantatkörpers, weil die Elastizitätsmodule von Knochen und Titan ähnlich sind.
Im Gegensatz zur Orthopädie, in der vornehmlich Titanlegierungen verwendet werden, werden moderne Zahnimplantate aus Reintitan hergestellt. Seit Jahrzehnten ist bekannt, dass sich Titan biologisch neutral (Biokompatibilität) verhält und keine allergischen oder Fremdkörperreaktionen auslöst. Das liegt daran, dass Titan eine direkte molekulare Verbindung mit dem Knochen eingeht. Bei anderen Materialien ist das nicht der Fall. Hierbei spielt die mikromorphologische Oberflächengestaltung eine Schlüsselrolle. Sie muss mit einer Mikro-Porentiefe von durchschnittlich 5µ bis 100µ aufgeraut sein.
Die Eigenschaft des Titans, mit Sauerstoff eine schützende Oxidschicht auf der Oberfläche zu bilden, ist die Ursache für sein bioinertes Verhalten und damit seine besonders gute Verträglichkeit. Die biologischen Eigenschaften des Knochens führen dazu, dass er eine direkte kristallographische Verbindung mit dem Titanoxid eingeht. Man nennt dies Osseointegration.
Eine weitere Voraussetzung für diesen biologischen Prozess ist die Anrauung der Titanoberfläche. Zu Beginn wurde dies durch Aufspritzen („additives Verfahren“) von Titanpulver unter Argon und Hochtemperatur erreicht (Titan-Plasma-Spray „TPS“).[3] Dieses Verfahren ist verhältnismäßig teuer, so dass viele Hersteller seit ca. 10 Jahren auf das billigere Säure-Ätz-Verfahren („acid etching“ oder Kombinationen davon, „SLA“ genannt) durch ein Gemisch von Salzsäure und Schwefelsäure zurückgreifen („subtraktive Verfahren“).
Gegenwärtig laufen zahlreiche Untersuchungen darüber, ob diese subtraktive Methode der Aufrauung der hervorragenden additiven Methode gleichwertig oder sogar überlegen gegenübersteht. Ziel ist in beiden Fällen die Anhaftung der Knochenbildungszellen (Osteoblasten) an der Oberfläche des aufgerauten Implantatkörpers, unabhängig von dessen äußerer Formgestaltung (Zylinder, Schraube, Blatt oder Disk).
In diese Beurteilung sind aber auch Marketing-Interessen der Hersteller im Hinblick auf ihre unique selling proposition, kurz USP, eingeflossen. Da beide Methoden unstreitig eine für medizinische Verhältnisse äußerst hohe Erfolgsquote (mehr als 95% bei einer fünfjährigen Verweildauer) haben, ist dies nicht von klinischer Bedeutung für den Patienten.
Alle Implantate müssen eine Zertifizierung der Gesundheitsbehörden als sichere Medizinprodukte (CE- oder FDA-Zulassung) besitzen.
Geeignete Patienten
Die Auswahl der geeigneten Patienten (Patientenselektion) war früher ein wichtiger Aspekt, weil man noch wenig über die Auswirkungen einer Implantation im Kieferknochen wusste. Heute kann in der Hand des erfahrenen Implantologen nahezu jeder Patient erfolgreich mit Implantaten behandelt werden. Im Vordergrund der Komplikationen stehen alle Faktoren, die eine Infektion begünstigen. So war man früher der Ansicht, dass Diabetiker nicht behandelt werden sollten, weil die Infektionsgefahr bei diesen Patienten größer ist. Inzwischen hat sich gezeigt, dass ein korrekt eingestellter Diabetes mellitus nicht nur allgemeinmedizinisch von großer Bedeutung ist, sondern auch gerade die Gefahr der Entzündungsneigung an den Zähnen auf ein erträgliches, beherrschbares Maß reduziert. Diabetiker sollten also nicht nur optimal eingestellt sein, sondern auch öfter zur Implantatkontrolle gehen.
Bei Patienten, die sich einer Chemotherapie unterziehen müssen, ist nicht nur die Immunabwehr eingeschränkt, sondern auch die Regenerationsfähigkeit des Gewebes während der Einheilungsphase nach der Implantation. Daher soll bei diesen Patienten die Beendigung der Chemotherapie abgewartet und erst einige Monate danach implantiert werden.
Bettlägerige Patienten können gegebenenfalls mit Implantaten versorgt werden, indem sie stationär ins Krankenhaus aufgenommen werden.
Seit einigen Jahren (etwa seit 1999/2000) ist eine unangenehme Erscheinung bei Patientinnen beobachtet worden, denen wegen ihrer Osteoporose ein bestimmtes, zunächst vielversprechendes Medikament von Orthopäden und Internisten verschrieben wurde. Es handelt sich hierbei um den Wirkstoff Bisphosphonat, der sich in mehreren im Handel erhältlichen Medikamenten befindet. Es wurde beobachtet, dass bei Patientinnen, die dieses Medikament einnehmen, nach zahnchirurgischen Eingriffen eine Atrophie (Rückbildung) des Knochengewebes in der Umgebung dieses Eingriffs festzustellen ist. Interessanterweise ist diese Atrophie selektiv im Bereich der Kieferknochen. Die Ursache hierfür ist noch nicht geklärt. Darüber hinaus wurde diese Erscheinung auch bei Patientinnen beobachtet, die wegen einer Krebserkrankung und der aufgetretenen Knochenmetastasen ebenfalls dieses Medikament zur Regeneration des Knochens bekamen. Ob es die Kombination von Chemotherapie mit Bisphosphonaten ist, die diese Erscheinung hervorruft, ist derzeit unbekannt. Zur Zeit gelten kieferchirurgische Eingriffe auch harmloser Art, wie z. B. Implantationen oder Extraktionen, bei gleichzeitiger Einnahme von Bisphosphonaten als kontraindiziert. Erschwerend kommt hinzu, dass man noch nicht genau abschätzen kann, wie lange Bisphosphonate benötigen, bis sie auch nach ihrer Absetzung ihre Wirkung im Knochen verlieren. Sie lagern sich ähnlich wie Tetracycline im Knochen ein. Hier kann es sich nach groben Schätzungen durchaus um 5 bis 10 Jahre handeln, da eine Hydrolysierung über Phosphatasen wegen der Molekülstruktur nicht erfolgt. Dieser Zeitraum stellt eine ernste Beschränkung dar und stellt die Verwendung von Bisphosphonaten grundsätzlich infrage.
Knochenquantität, knochenvermehrende Maßnahmen („Knochenaufbau“) und Knochentransplantate
Wenn nicht genug Knochen vorhanden ist, z. B. nach langjähriger Tragedauer einer herausnehmbaren Zahnprothese, kann eventuell ein Implantat normaler Größe nicht eingesetzt werden. Dann muss entweder ein kleineres Implantat gewählt werden (zum Beispiel ein kürzeres Zylinderimplantat, ein schmales Blattimplantat oder ein Miniimplantat) oder der benötigte Knochen muss durch geeignete chirurgische Maßnahmen aufgebaut werden. Dies kann entweder mit synthetischem Knochenersatzmaterial (z. B. Tricalciumphosphat, TCP), das dem Knochen sehr ähnlich ist, geschehen oder durch Schaffung eines geschlossenen Hohlraums, in den dann Knochensubstanz einwachsen kann (sich regeneriert), ähnlich wie bei einem leeren Zahnfach nach einer Zahnextraktion (Zahnentfernung). Im Prinzip wächst Knochengewebe genauso nach wie Weichgewebe. Er benötigt wegen seiner geringeren Stoffwechselrate jedoch sehr viel länger dafür. (Die vollständige Knochenregeneration beim Menschen beträgt ca. 10 Jahre, während z. B. die Regeneration aller Leberzellen nur ca. 6 Monate dauert und die der Darminnenauskleidung (Epithel) schon nach 3 Tagen komplett ist[4])
Fremdmaterial, und dazu gehört auch körpereigener Knochen aus anderen Bereichen des Skeletts, z. B. aus der Hüfte, verhält sich im Grunde wie synthetisches Material. Es kann daher auch nur als Platzhalter wirken, weil es ebenfalls zunächst vom Körper (über einen Zeitraum von etwa einem Jahr) abgebaut werden muss, bevor der genetisch für diesen Ort im Kiefer des Körpers geeignete Knochen entstehen kann.[5] Warum selbst körpereigener Knochen abgebaut und nicht umgewandelt wird, liegt auf der Hand: jeder Gewebetyp bei Tieren und Menschen braucht für das Wachstum seiner Zellen Boteneiweiße, die das Wachstum und die Teilung von Zellen in der Nachbarschaft auslösen. Bloße Zufuhr von Nahrungsstoffen, wie bei Bakterien (Prokaryoten) führt bei Mensch und Tier (Eukaryoten) nicht zu Zellwachstum und Zellvermehrung. Daher ist es sinnlos, wenn unter der Vorstellung der Beschleunigung des Anwachsens nach einer Implantation Calciumtabletten gegeben werden. Dieses Calcium wird als Überschuss rasch über die Nieren ausgeschieden.
Fremdmaterialien und eben auch körpereigene Knochentransplantate kommen aus einer Körperregion, in der im System der Boteneiweiße andere Empfängerstellen (Rezeptoren) an den Nachbarzellen sind. Das Transplantat sendet also, solange es lebt, Boteneiweiße aus, für die die Nachbarschaft der Zielregion (hier der Kieferknochen) keine Rezeptoren hat; und umgekehrt: die Nachbarzellen senden Boteneiweiße aus, die im Transplantat keine Empfänger finden[6] Das Transplantat ist aus dem Messenger-Receptor-System ausgekoppelt. Bis zu seinem Absterben und der Resorption vergeht aber eine verhältnismäßig lange Zeit, so dass es zunächst bis zu seinem Verschwinden (ca. 1-2 Jahre) als Platzhalter dienen kann. Anders als bei völlig fremden Transplantaten (Niere, Herz, Leber) von anderen Menschen oder Tieren kommt es aber nicht zu der dort bekannten heftigen immunologischen Abwehr.
Insofern bedeutet der Einsatz von Fremdmaterial immer eine Verzögerung des Nachwachsens eigenen Knochens. Wenn also irgendmöglich, sollte das zunächst störende Material nicht eingesetzt werden. Nur wenn ausreichend Zeit ist (ca. 1 Jahr und mehr), kann auch synthetisches Knochenersatzmaterial als Platzhalter eingesetzt werden.
Eine routinemäßig verwendete Methode zur Verdickung der Knochenschicht im Seitenzahnbereich des Oberkiefers ist der Sinuslift. Hierunter versteht man eine Operationsmethode, bei der die Schleimhaut des Kieferhöhlenbodens abgelöst und der entstehende Hohlraum durch Knochenersatzmaterial oder auf natürliche Weise (Umwandlung des Blutkoagels in nativen (gewachsenen) Knochen) aufgefüllt wird. Hierbei kann dann das Implantat gleichzeitig eingesetzt werden oder zu einem späteren Zeitpunkt, wenn die für die Implantatlänge erforderliche Schichtdicke an Knochen nachgewachsen ist. Je kürzer hierbei das Implantat sein kann, desto schneller ist das Ziel erreicht. Deshalb eignen sich für den Sinuslift oft die kurzen, aber dafür horizontal ausgerichteten Blattimplantate mit geringer Eindringtiefe. Werden sie zudem gleichzeitig, aber belastungsfrei (durch Abschrauben der Trägerpfosten) mit dem Sinuslift in den Kieferknochen oder der restlichen Knochenschicht in Position gebracht, dient ihre mikroporös aufgeraute Titanoberfläche als erste wichtige Haftfläche für Knochenzellen, so dass die Knochenneubildung auf diese Weise auch von der Implantatoberfläche ausgehen kann.
Knochenqualität
Es gibt keinen „schlechten Knochen“, sondern nur dichten oder weniger dichten (Spongiosa), schwammigen Knochen. Dieser ist mit zahlreichen Hohlräumen durchsetzt, so dass der mechanische Kontakt zum Implantat geringer ist als beim dichten Knochen der Knochenaußenschicht (Compacta). Die Spongiosa ist ein wichtiger Ort der Knochenneubildung und vor allem der Blutbildung. Für den Halt eines Implantates ist dieser Gewebetyp aber nur bedingt geeignet und zeigt für Implantate mit wenig Oberfläche wenig Haftungsmöglichkeit. Hier eignet sich das flache blattförmige Implantat deutlich besser (wegen seiner 4-fach größeren Oberfläche im Vergleich zu seinem Volumen). Bei Verwendung dieses Implantattyps gibt es daher keinen Unterschied zwischen Oberkiefer und Unterkiefer.
Besonderheiten der Knochenbiologie im Frontzahnbereich
Die Ernährung des Gewebes erfolgt im Wesentlichen über die Blutzufuhr. Im Oberkiefer geschieht dies hauptsächlich durch zwei große Arterien (Arteria palatina), die vom hinteren Rand in der seitlichen Kerbe des Oberkiefers beiderseits nach vorne ziehen. Somit wird der Gaumen gut durchblutet, während die vestibuläre Seite des Knochens durch die Zahnreihe hindurch und die wangenseitige Schleimhaut ernährt werden muss. Diese relative Mangelernährung des Knochens auf der Wangenseite führt auch unter natürlichen Umständen dazu, dass sich die Kontur der Zahnwurzeln in der knöchernen Unterlage des dortigen Zahnfleisches abbildet, vor allem im Eckzahnbereich gut sichtbar. Aus diesem Grunde kann es im Frontzahnbereich nach einer Implantation dazu kommen, dass sich die dünne Alveolenwand zurückbildet, und mit ihr auch das Zahnfleisch. Dies hat unangenehme kosmetische Effekte, so dass man den metallisch-dunklen Implantatkörper, besonders beim Lachen sehen kann.
Um hier Abhilfe zu schaffen, besann man sich wieder auf die weißen Keramiken, die früher verwendet wurden. Seinerzeit wurden diese Werkstoffe verlassen, weil sie nicht elastisch genug waren und unter der Durchbiegung des Knochens oftmals in der Tiefe brachen. Seit einiger Zeit gibt es ein extrem hartes Material, das Zirkon, das diesen Belastungen standhält und wegen seiner weißen Farbe bei einer eventuellen Rückbildung des Knochens und des Zahnfleisches kosmetisch nicht so störend ist. Leider geht diese Keramik keine dem Titan vergleichbare Verbindung mit dem Knochen ein. Die Erfahrungen mit diesem Werkstoff sind noch nicht ausreichend, um wirklich als Alternative zum Titan zu gelten. Hier muss noch abgewartet werden.
Da es sich bei der Rückbildung des Knochens in der Front um ein Ernährungsproblem handelt, lässt sich dieses Problem jedoch lösen, wenn man ein schmaleres oder anders geformtes Implantat nimmt. Neben den hierfür besonders gut geeigneten Blattimplantaten (diese Auffassung ist weitgehend veraltet) gibt es einen, ebenfalls zylindrisch geformten Implantattyp, der sich dadurch auszeichnet, dass er wie eine Säule von Geldmünzen mit großen Abständen zueinander aussieht. Der Kern ist dabei sehr dünn. Diese Konstruktion hat den Vorteil, dass vor allem in waagerechter Richtung die Ernährung des Knochens gewährleistet ist. Außerdem ist sein oberer Rand kegelförmig abgeschrägt und entspricht damit in der Kontur eher dem zugespitzten Kieferkamm. Dadurch bleibt die Knochenschicht am oberen Rand sehr viel dicker und kann das Zahnfleisch besser ernähren. Der Rückgang des Knochens und der Gingiva im ästhetisch besonders wichtigen Bereich der Front ist somit weniger wahrscheinlich.
Die Ernährung des Knochens in den empfindlichen Frontzahnbereichen wird auch vermindert, wenn zu viele Implantate dort eingesetzt werden, z. B. für jeden fehlenden Zahn ein Implantat. Im Gegensatz zum natürlichen Zahn, bei dem eine Ernährungswechselwirkung zwischen Zahn und dem ihn umgebenden Knochen existiert (Tarnow, New York University), fehlt diese Ernährung beim Implantatkörper. Vor allem der dünne Knochenspalt zwischen den Implantaten führt oft dazu, dass sich dieser „Restknochen“ nicht selbst ernährt und dann zugrunde geht. Es kommt also auf das richtige Verhältnis von lebender Substanz zu toter Fremdsubstanz an. Wird der Kieferknochen durch zu viel metallische Fremdsubstanz ersetzt wie bei dicken Implantatzylindern, die zudem auch noch sehr eng stehen, zieht er sich wegen Mangelernährung zurück. Wie dieser Quotient zwischen Knochensubstanz und Metall aber aussehen muss, ist bisher noch nicht definiert und ist damit Gegenstand zukünftiger Untersuchungen. Für den minimalen Abstand zwischen Implantatkörper und ihren die zukünftige Zahnkrone tragenden Pfeilern gilt ein Erfahrungswert von 1,5 bis 2 mm im oberen Bereich an der Durchtrittstelle durch das Zahnfleisch, und zwar rundherum, also auch lippenseitig. Dieser Wert muss verhältnismäßig oft in der Front unterschritten werden, zumal das natürliche Zahnfach (Alveole) genau dort oft weniger als 1 mm Randdicke hat. Sehr oft zieht sich das Zahnfleisch auch beim natürlichen Zahn gerade dort zurück, wo man es am meisten sieht (scheinbar lange Zähne). Das Implantat vergrößert das Problem.
Abhilfe könnte hier eine ovale statt kreisrunde Implantatform schaffen, wie sie ja auch beim natürlichen Frontzahn gegeben ist. Diese ovale Form würde die Knochenschicht zwischen den Implantaten verbreitern, wenn sie jeweils so gedreht werden, dass die schmalen Kanten nach außen und innen ausgerichtet werden. Damit wäre aber das Problem der zu dünnen knöchernen Außenschicht (lippenseitigen) des Implantatlagers weiterhin ungelöst. Das Einbringen dieses ovalen Implantates wäre außerdem für den Behandler schwieriger als bei einem kreisrunden Implantat.
Zweifellos gibt es trotz enormer Erfolge bei Implantaten im Mundbereich noch zahlreiche Verbesserungsmöglichkeiten.
Operationstechnik einer Implantation
Eine zahnärztliche Implantation wird bei örtlicher Anästhesie ambulant durchgeführt und verläuft schmerzfrei. An der geplanten Stelle wird die Schleimhaut zur Seite gelegt und das Implantatbett stufenweise nach individuell festgelegter Länge und Durchmesser aufbereitet. Zur Vermeidung einer Überhitzung des Knochen wird die Präparation mit geringer Drehzahl des rotierenden Instrumentes und permanenter Kühlung mit physiologischer Kochsalzlösung ausgeführt. Nach dem Einbringen wird das Zahnfleisch wieder vernäht. Bei guter Nachsorge (Kühle Umschläge, Medikamente) lassen sich Komplikationen (Schwellungen usw.) weitgehend verhindern. Nach zehn Tagen ist die Wundheilung normalerweise abgeschlossen. Eine unbelastete Einheilphase, abhängig von der Knochenqualität, schließt sich an. Diese beträgt durchschnittlich 2-3 Monate im Unterkiefer und 5-6 Monate im Oberkiefer, da die Knochendichte von Unter- und Oberkiefer unterschiedlich ist.
Für diese Übergangszeit wird ein provisorischer Zahnersatz eingesetzt. In Ausnahmefällen kann das Implantat auch schon früher belastet werden. Dies ist jedoch von der Knochenqualität und dem geplanten Zahnersatz abhängig.
Bei einem mehrteiligen Implantat wird nach der Einheilphase das Gewinde des Implantatkörpers wieder frei gelegt, die Implantat- Hals- und -Kopfteile eingeschraubt und die Suprakonstruktion gefertigt und eingegliedert. Auf einem einteiligen Implantat kann nach der Einheilphase die Suprakontruktion unmittelbar eingegliedert werden.
Bei einem minimal invasiven Vorgehen wird das Implantatbett für das Miniimplantat präpariert ohne einen Schleimhaut-Periost-Lappen zu bilden. Orientierungshilfe bietet eine Bohrschablone. Das Sofortimplantat, das ein selbstschneidendes Gewinde hat, wird mit Hilfe eines Drehmomentschlüssels eingebracht. 55 Ncm sollen dabei erreicht werden, um die nötige Primärstabilität zu erreichen. Die vereinfachte und kürzere Operation verringert die Angst des Patienten und die postoperativen Beschwerden. Möglicherweise liegt hier die Zukunft der Zahnimplantation.
Nachsorge
Unmittelbar nach einer implantologischen Versorgung soll die Operationsstelle nicht belastet werden. Auch zu intensive Reinigungsmaßnahmen (z. B. mit einer harten Zahnbürste) direkt an der Naht sind zu vermeiden, wohingegen das restliche Gebiss sehr sorgfältig gereinigt werden muss. Als zusätzliches Hilfsmittel stehen Chlorhexidin oder Listerine als Mundspüllösungen zur Verfügung. So kommt der Infektionsprophylaxe in den ersten 48 Stunden nach der Operation eine Schlüsselrolle zu. Wichtig ist auch, möglichst keine Prothesen im Operationsgebiet zu verwenden oder diese „hohl zu legen“, weil diese andernfalls unkontrollierte Belastungen auf das Implantat übertragen könnten. Die Dauer der Einheilphase bis zur direkten Belastung des Implantates wird wissenschaftlich derzeit noch diskutiert - mit tendenziell abnehmender Dauer (siehe auch Belastungszeitpunkt) bis hin zur Sofortbelastung.
Zahnimplantate müssen wegen der Infektionsgefahr regelmäßig kontrolliert werden. Rechtzeitig erkannte Infektionen sind deutlich erfolgreicher zu behandeln als fortgeschrittene, die bereits zu einem Abbau von Knochenmaterial geführt haben. Daher sollen Zahnimplantate alle 6 Monate vom behandelnden Zahnarzt bzw. Implantologen kontrolliert werden. In klinischer Erfahrung hat sich gezeigt, dass es insbesondere bei großen kieferchirurgisch-implantologischen Maßnahmen in beiden Kiefern sinnvoll sein kann, den Patienten nach dem Eingriff kurz stationär nachzuversorgen, z. B. bei großvolumigen Knochenaufbauten mit Knochentransplantationen aus der Hüfte oder mit Knochenersatzmaterial. Kernpunkt dieser postoperativen Nachsorge ist die Ernährung über einen Venenkatheter, um eine bakterielle Gefährdung der frischen Operationswunden im Mund durch die normale orale Nahrungsaufnahme zu vermeiden.
Behandlungszeitpunkt
Man unterscheidet zwischen Sofortimplantaten direkt nach Zahnverlust, verzögerten Sofortimplantaten 4–8 Wochen nach Zahnverlust, und Spätimplantaten nach vollständiger Verknöcherung des Zahnfachs. Sofortimplantate sollten nur eingesetzt werden, wenn direkt nach der Extraktion des Zahnes die Alveole entzündungsfrei ist. Verzögerte Sofortimplantationen und Spätimplantationen verringern dieses Risiko. Bei einwurzeligen Zähnen in Regionen mit dünnen vestibulären Knochenlamellen (z. B. im Frontzahngebiet) hat die Sofortimplantation oder verzögerte Sofortimplantation (hier: innerhalb von 2 Wochen) jedoch den entscheidenden Vorteil, dass der Knochenverlust und damit das Risiko eines ästhetischen Misserfolgs, minimiert wird.
Sofortimplantationen kommen den Bedürfnissen des Patienten am nächsten, bergen aber auch das größte Verlustrisiko.
Belastungszeitpunkt
Neben dem Operationszeitpunkt nach einer Zahnentfernung ist auch der Belastungszeitpunkt des Implantates von Bedeutung. Man unterscheidet die Sofortbelastung von der Spätbelastung. Die Sofortbelastung setzt Primärstabilität (hohe Festigkeit des Implantates schon bei der Operation) voraus und bedeutet die sofortige Versorgung des Implantates mit der belastenden Suprakonstruktion (Krone, Brücke, herausnehmbare Prothese). Demgegenüber ist für die Spätbelastung die Primärstabilität nicht entscheidend, weil der Knochen in der Einheilzeit (mehrere Wochen bis Monate) das Implantat immer fester umschließt. Je geringer die Primärstabilität des Implantats bei der Operation ist, desto mehr Zeit muss für die Bildung der ausreichenden Knochensubstanz eingeräumt werden. Über die (in Ncm Eindrehmoment) gemessene Primärstabilität gibt es erst seit 2006 Standards, über die man sich unter Implantologen in Konsensuskonferenzen einigen konnte. Noch nicht einig hingegen sind sich die Implantologen in der Frage, ob eine Einheilphase vonnöten ist. Moderne Systeme ermöglichen eine sofortige Belastung. Dabei muss eine ausreichende Knochendichte vorhanden sein.
Verweildauer
Die Verweildauer (laienhaft auch als „Haltbarkeit“ bezeichnet) der Implantate im Kiefer ist abhängig vom Erhalt des umgebenden Knochens. Die Verbindung zwischen Implantat und Knochen ist nahezu ausschließlich durch bakterielle Einflüsse zerstörbar (Auflösung der Knochenmatrix durch Matrixmetalloproteinasen, MMPs). Genetische Gesichtspunkte der evolutionsbiologisch verhältnismäßig jungen Ernährung mit Getreideprodukten erklären die erhöhte Infektionsneigung der Gingiva und des Zahnhalteapparates bei schwerpunktorientierter Broternährung in Deutschland. Daher kommt der Infektionsverhütung vor, während und nach dem Einbringen des Zahnimplantates eine entscheidende Rolle zu. Mit abnehmender Empfindlichkeit gegenüber bakteriellen Einflüssen bei gleichzeitiger Zunahme des intensiven Implantat-Knochenkontaktes (BIC: bone to implant contact) unter funktionell-physiologischer Kaubelastung sinkt das Risiko des Implantatverlustes, weil die mechanische Belastung zeit- und intensitätsabhängig zu einer röntgenologisch nachweisbaren gesteigerten Mineralisierung des umgebenden Knochens führt. Dies bedeutet, dass in der Anfangszeit nach der Operation sehr viel größere Aufmerksamkeit auf Zahnreinigung und Mundhygiene verwendet werden muss, als z. B. nach ca. 2 Jahren ereignisloser Tragezeit. Die Verweildauer ist außerdem abhängig von der Größe der implantatgeometrisch bedingten Oberfläche, von der mikromorphologischen Gestaltung und von der äußeren Form.
Die Erfolgssicherheit zylindrisch orientierter Implantate liegt nach internationalen Statistiken im 5-Jahresintervall bei 85-90%. Sie ist im Wesentlichen vom Eintreten einer Infektion abhängig. Durch geeignete Maßnahmen, die sich der konsequenten Infektionsprophylaxe unmittelbar postoperativ durch stationäre Nachsorge zuwenden, ist es daher möglich, die Erfolgsquote im 10-Jahresintervall auf nahezu 100% zu steigern. Dies gilt nur für Nichtraucher. Es sind Liegezeiten von mehr als 40 Jahren bekannt.
Mit diesen Zahlen gehört die zahnärztliche Implantologie zu den erfolgreichsten medizinischen Eingriffen überhaupt. Die Erfolgsquoten im Bereich der orthopädischen Implantate liegen mit 75 bis 85% deutlich darunter. Die Gründe liegen in der erhöhten Elektivität zahnärztlicher Implantate. Auch den endogenen Infektionsfaktoren widmet sich die zahnärztliche Implantologie intensiver. Bei orthopädischen Implantaten ließe sich zudem durch verschiedene Änderungen der mikro- und makromorphologischen Aspekte die Erfolgsquote steigern.
Erfolg und Misserfolg
Zahnimplantate können nicht von Karies befallen werden, aber sie können eine periodontale Erkrankung aufweisen, die Periimplantitis bezeichnet wird (eine Entzündung des Gewebes um das Zahnimplantat herum). Die Ursache ist entweder auf nicht sterile Verhältnisse während der Operation oder auf eine ungenügende Mundhygiene des Patienten zurückzuführen. In jedem Fall führt dies zu einer Atrophie (Gewebsschwund) des Knochens, die letztendlich den Ausfall des Zahnimplantats bewirkt.
Der Erfolg einer Implantation beruht auch auf den Fähigkeiten des operierenden Arztes und vor allem auf der Qualität und Quantität des Knochens und auf deren richtiger Einschätzung.
Ein Zahnimplantation wird als Misserfolg angesehen, wenn das Implantat mobil ist oder einen periimplantären Gewebsschwund von mehr als 1 mm im ersten Jahr aufweist.
Eine Periimplantitis wird oft mit der Gabe von Antibiotika vor und nach der Implantation präventiv behandelt. Eine Periimplantitis ist gut auf einer Panoramaröntgenaufnahme (OPG) zu erkennen.
Das Risiko eines Misserfolges ist bei Rauchern erhöht. Deshalb wird in vielen Praxen nur dann eine Implantation durchgeführt, wenn der Patient Nichtraucher ist (bzw. sich das Rauchen abgewöhnt hat). Ein Misserfolg kann aber auch dann auftreten, wenn die Position des Zahnimplantats nicht richtig ist. Allerdings kann eine falsche Positionierung durch eine 3D-unterstützte Implantation vermieden werden. Mit Hilfe einer CT(Computertomographie)- oder DVT(Digitales Volumen Tomogramm)-Aufnahme und entsprechender Software kann die künftige Position des Implantats, schon vor dem Eingriff exakt festgelegt werden. Die Planung erfolgt dreidimensional am Computer und wird anhand einer individuell hergestellten Bohrschablone umgesetzt. Nachteilig hierbei sind Strahlenbelastung und zusätzliche Kosten für den Patienten.
Faktoren von Einfluss
Folgende Faktoren sind zusammenfassend für eine erfolgreiche implantologische Behandlung von Bedeutung:
- Patientenselektion, d. h. die allgemeinmedizinischen und lokalen Indikationen müssen überprüft werden
- Knochenquantität, d. h. es muss genug Knochen da sein; die Kieferhöhle und der Nasenboden im Oberkiefer, sowie der Nervkanal im Unterkiefer und die Kieferkammbreite in beiden Kiefern sind begrenzende anatomische Faktoren
- Knochenqualität, d. h. ein bestimmtes Implantatsystem benötigt eine bestimmte Knochenqualität: ein Extensionsimplantat ist im schwammig-lockeren Knochen des Oberkiefers erfolgreicher als ein zylinderförmiges Implantat
- Implantatmaterial, d. h. das Implantat muss ein dem Knochen ähnliches Elastizitätsmodule haben und seine Oberfläche biologisch kompatibel sein – Titan erfüllt beide Bedingungen
- Implantatoberfläche, d. h. die Oberfläche muss mikroporös sein (5 bis 100 Mikrometer Porendurchmesser), damit sich Knochenzellen anlagern (eine Eigenart aller Bindegewebszellen)
- Implantatform, es gibt Blatt-, Nadel-, Schrauben-, Zylinder- und konische Implantate. Unterschiedliche Implantate haben unterschiedliche Indikationen. Diese bestimmen sich über das Knochenangebot, die Knochenqualität und das erstrebte Funktionsziel. Die richtige Auswahl hat der Behandler zu treffen
- Implantationsplanung, das Implantat soll möglichst so stehen, dass später eine Zahnkrone optimal positioniert ist, der Halt einer herausnehmbaren Prothese funktionell störungsfrei möglich wird und schließlich die Knochenernährung unbeeinträchtigt bleibt
- chirurgisches Vorgehen, der Erfolg hängt von der Erfahrung, der Ausbildung und der zur Verfügung stehenden Ausrüstung des Operateurs ab. Hierbei steht die sterile Vorgehensweise im Vordergrund, es sollte möglichst wenig biologische Substanz dem Implantat geopfert werden und schließlich darf der Knochen beim Präparieren des Implantatlagers nicht überhitzt werden (Kühlung)
- Suprakonstruktion, der Erfolg hängt von dem ab, was auf das Implantat gesetzt wird: (festsitzende Brücken oder herausnehmbare Zahnprothesen). Bei festen Brücken/Kronen haben Implantate eine höhere Verweildauer
- Okklusion, das Implantat sollte möglichst wie ein Zahn normal belastet und ebenso nicht überbelastet werden
- Mundhygiene, das Implantat (besser: die Kronen/Zähne darauf) muss wie ein normaler Zahn gepflegt werden, um eine Entzündung des Zahnfleisches (Frühsymptom: Blutung) und später des das Implantat tragenden Knochens zu vermeiden
- Nachsorge, regelmäßige Kontrolle (alle 6 Monate) der Mundhygiene und des Implantates durch den Zahnarzt, regelmäßige, individuell abgestimmte professionelle Zahnreinigungen (2- bis 4-mal jährlich).
Ein Abweichen von diesen Faktoren bedeutet eine Zunahme der möglichen Komplikationen.
Entwicklungen der Implantologie
Sofortimplantate
Seit einigen Jahren geht der Trend zu Sofortimplanten und damit zu Implantatformen, deren unteres Ende verjüngt ist (konische Schraubenimplantate). Diese Implantatgeometrie kommt der natürlichen Wurzelform am nächsten und scheint insbesondere bei Sofortimplantationen sinnvoll, um die vorhandenen knöchernen Strukturen zu schonen, die zylinderförmigen, parallelwandigen Implantate gewährleisten aber eine bessere Primärstabilisierung weil im Bereich der Spitze des leeren Zahnfachs eine höhere Friktion erreicht wird.
Operationstechnisch sind konische, wurzelförmige Implantate zudem mit dem Nachteil behaftet, dass die Einsetztiefe durch die Form des Implantats nicht variabel ist und somit den gegebenen anatomischen Verhältnissen nicht immer ausreichend angepasst werden kann. Durch die zunehmende Zahl verschiedener Durchmesser und Längen der Implantate lässt sich aber auch bei konischen Implantaten eine befriedigende primäre Stabilität erreichen.
Weiterentwicklung der Materialien
Wegen kosmetischer Probleme bei einer Rückbildung des Zahnfleisches und des Knochens hat man sich seit etwa 5 Jahren auf Zirkon als Implantatmaterial besonnen. Keramiken zeichnen sich durch eine dem Titan vergleichbare Gewebsverträglichkeit aus. Titan steht durch die Vertreter der Zirkon-Implantate in der Diskussion, durch eine Metallintoxikation Reaktionen auszulösen (zum Beispiel Lymphozyten-Transformationstest). Inwiefern diese Reaktionen aber zu klinischen Beeinträchtigungen führen und es daher sinnvoller ist, die Vorteile von Titan als Werkstoff aufzugeben, kann noch nicht abschließend beurteilt werden. Hierbei ist zu bedenken, dass Titan über seine diversen Verbindungen natürlicher Bestandteil des Organismus ist, so dass der „Lymphozyten-Transformationstest“ nicht die erforderliche Spezifität hat. Auch gibt es noch keine wissenschaftlichen Untersuchungen zur Höhe des Ausdrehmomentes, einer Größe, die Aufschluss über den Osseointegrationsgrad des Implantatkörpers gibt. Jüngere Erfahrungsberichte zeigen jedoch umfangreiche knochenauflösende Entzündungen und eine Verlustquote von über 50% im 2-Jahreszeitraum. Diese Zahlen sind im Vergleich zur Verwendung von Titanimplantaten völlig inakzeptabel und sind schon vor Jahren Grund für das Ende der sogenannten "Tübinger" oder "Münchner" Implantate gewesen. Auch diese waren aus Keramik und hatten eine Misserfolgsquote von über 30%, weil der dem Titankristall innewohnende Mechanismus der reversiblen ionischen Einbindung des Knochen-Calciums bei Zirkon und anderen Keramiken fehlt. Diese Einbindung ist bakteriendicht.
Auch versucht man, die guten Erfahrungen mit Keramiken bei der Knocheneinheilung durch Beschichtung der Implantate mit knochenverwandten Stoffen (künstlichem Knochenmineral, d. h. Hydroxylapatit) oder TCP (Tricalziumphosphat) zu verbessern. Diese Versuche zeigten bisher keinen Vorteil im Hinblick auf eine beschleunigte Osseointegration. Im Gegenteil führte das Hydroxylapatit zu Einschmelzungen am Knochenlager mit folgendem Implantatverlust. Auch Tricalziumphosphatbeschichtungen brachten bisher im Hinblick auf eine schnellere „Einheilung“ keine Vorteile gegenüber der reinen Titanoberfläche.
Neuere Ansätze beschichten die Implantat-Oberfläche mit (Proteinen (Eiweißen), die die Knochenbildung am Implantat anregen und fördern sollen. Ob diese Versuche sich letztlich durchsetzen und ob sie eine Beschleunigung der Osseointegration bewirken, muss abgewartet werden. Die noch ungeklärte Gesamtwirkung dieser speziellen Proteine (Zytokine) auf andere Bereiche der Biologie des Organismus setzt ein deutliches Fragezeichen hinter diese Versuche, weil es erste Hinweise auf fatale Leberschäden gibt. Die hier verwendeten Zytokine, vor allem das BMP 2 haben keineswegs nur eine spezielle knochenfördernde Wirkung, sondern wirken an anderer Stelle als Auslöser von gesteuertem Zelluntergang (Apoptose). Deren Wirkung wird vor allem durch den Einfluss der Blutverdünnung durch Heparin noch deutlich (20-fach) verstärkt. [7]
Letztlich gibt es jedoch bei der inzwischen festzustellenden Erfolgsquote von durchweg über 95% der gängigsten Implantattypen ohne künstliche Mineral- oder Proteinauflagerung kaum noch etwas zu verbessern. Die Ursachen der restlichen 3-4% Verlust lassen sich wissenschaftlich nicht auf die Oberflächengestaltung oder die Form des Implantates zurückführen.
Implantate und Zahnersatz - Suprakonstruktionen
Zahnimplantate und festsitzender Zahnersatz
Hierbei werden auf den (meist abschraubbaren) Pfeilern der Implantate Einzelkronen oder Brückenpfeiler zur Schließung einer Zahnlücke durch eine Brücke festgeschraubt oder einzementiert.
Indikationen:
- Einzelzahnersatz oder kleine Schaltlücke (1-2 fehlende Zähne der sonst geschlossenen Zahnreihe)
- Große Schaltlücke (mehr als 2 fehlende Zähne der sonst geschlossenen Zahnreihe)
- Freiendsituation (verkürzte Zahnreihe) (festsitzender Zahnersatz nur bedingt möglich)
Einzelzahnersatz oder Schließen einer kleinen Zahnlücke
Ca. 10-20% aller Implantatfälle haben diese Indikation.
Gründe für den Zahnverlust können sein:
- Karies
- Parodontitis oder Parodontose
- unfallbedingter Zahnverlust (Trauma)
- Nichtanlage von Zähnen
Bei der Nichtanlage von Zähnen muss eine intensive Abstimmung mit einem Kieferorthopäden erfolgen.
Beim Einzelzahnersatz oder Schließen einer kleinen Schaltlücke müssen zum Unterschied zur Alternativ-Versorgung mit einer Brücke die Nachbarzähne nicht beschliffen werden. Kronen können direkt auf das Implantat/die Implantate gesetzt werden. Das Zahnfleisch legt sich bei einer optimalen Ausgangssituation harmonisch an die Kronen an und nichts deutet mehr auf den Zahnverlust hin. Es ist allerdings sehr oft der Fall, dass durch chirurgische Eingriffe ein sogenanntes Weichgewebsmanagement durchgeführt werden muss, um einen ästhetischen Übergang von Zahn zu Zahnfleisch zu erreichen - vor allem im sichtbaren Frontzahnbereich.
Probleme beim Einzelzahnersatz können sich ergeben, wenn die Zahnlücke nicht hinreichend groß ist - bei zu kleinem Interdentalabstand. Bis ca. 2003 bemühte man sich möglichst lückenfüllende Implantatdurchmesser einzusetzen, um ein ästhetisches Ergebnis zu erzielen. Heute liegt der Schwerpunkt jedoch darauf, einen ausreichenden Mindestabstand von benachbarten Wurzeln natürlicher Zähne einzuhalten.
Große Schaltlücken
Von großen Schaltlücken spricht man, wenn mehrere Zähne nebeneinander fehlen, endständig aber mindestens noch ein Zahn vorhanden ist.
Um eine solche Lücke mit festsitzendem Zahnersatz zu schließen, bestehen (soweit eine „normale“ Brücke nicht mehr möglich ist) folgende Möglichkeiten:
- Je zu ersetzendem Zahn wird ein Implantat eingesetzt und jeweils mit einer Krone versehen (sehr aufwändig und kostenintensiv).
- Es werden mindestens zwei Implantate als Brückenpfeiler eingesetzt, bei sehr großen Lücken auch mehr als zwei. Auf diesen Implantaten wird dann eine Brücke befestigt. (Implantatgetragene Brücke)
- Implantate und natürliche Zähne dienen gemeinsam als Brückenpfeiler (Hybrid-Brücke). Das ist nur in Ausnahmefällen zu empfehlen, weil ein Implantat keine Bewegung zulässt, natürliche Zähne innerhalb gewisser Toleranzgrenzen aber sehr wohl. (Siehe Zahnhalteapparat)
Freiendsituation
Freiendsituation heißt, dass im distalen Bereich kein natürlicher Brückenpfeiler mehr vorhanden ist, der eine Brücke tragen könnte.
Durch entsprechend platzierte Implantate ist dann festsitzender Zahnersatz (eine Brücke) möglich.
-
- Ein Beispiel für eine Freiendbrücke auf 2 Implantaten
Eingegliederte Freiendbrücke 35-37 von okklusal (in der Aufsicht)
Freiendbrücke mit Keramikverblendung, von bukkal, über einen Spiegel fotografiert
Zahnimplantate und herausnehmbarer Zahnersatz
Implantatpfeiler können ebenso auch der Verankerung herausnehmbarer Teilprothesen dienen, die sich mittels Doppelkronen, Stege, Geschiebe, druckknopfähnlicher Kugelköpfchen, ja sogar Magneten an den Implantaten befestigen lassen: Kombinierter Zahnersatz
Indikationen:
- Verankerung Kombinierten Zahnersatzes
- Verankerung von Deck- oder Cover-Denture-Prothesen (auch Hybridprothesen genannt) bei zahnlosem Kiefer
Stark reduzierte Bezahnung
Von einer starken Reduzierung der Bezahnung in einem Kiefer spricht man, wenn etwa nur noch 5-6 eigene Zähne vorhanden sind. Die Beurteilung, wann eine Bezahnung als stark reduziert einzustufen ist, ist aber auch sehr von der Verteilung der Restbezahnung abhängig, ob nur Frontzähne, einseitige oder beidseitige Restbezahnung.
In einem derartigen Gebiss dienen Implantate dazu, die Anzahl der Pfeiler zu vermehren, um eine bessere Abstützung und einen sichereren Sitz einer Prothese oder herausnehmbaren Brücke zu gewährleisten. Eine Befestigung mittels Teleskopkronen ist in diesen Fällen eine optimale Lösung.
Totalersatz - Zahnloser Kiefer
Diese Indikation betrifft ca. 60% aller Implantatfälle.
Viele Prothesenträger klagen über einen schlechten Sitz ihrer Prothese oder schmerzhafte Druckstellen. Haftmittel oder mechanische Hilfen lösen diese Probleme oft nicht zufriedenstellend.
Implantate sind in diesen Fällen das Mittel der Wahl. Der Tragekomfort einer Prothese kann so erheblich verbessert werden, wobei gilt: Je mehr Implantate, um so höher der Tragekomfort.
Diese Lösung wird im zahnlosen Unterkiefer häufiger als im Oberkiefer eingesetzt, weil Unterkieferprothesen auch häufiger Probleme bereiten. Im Unterkiefer reichen eventuell 2 Implantate (besser 4), im Oberkiefer sollten aufgrund der weicheren Knochenstruktur mindestens 4 Implantate eingesetzt werden.
Die Implantate können über Stegverbindung (evtl. sogar mit Friktionshilfen) miteinander verbunden werden. Das dient sowohl der Stabilisierung der Implantate als auch der besseren Prothesenverankerung. Aufgrund der hohen Primärstabilität ist eventuell auch eine Sofortbelastung möglich.
Sind etwa 6 bis 8 Implantate vorhanden, kann eine Prothese allein auf diesen abgestützt werden. Eine Belastung der Kieferkämme entfällt dann, so dass kein Knochenabbau zu befürchten ist.
Stehen noch mehr Implantate als Pfeiler zur Verfügung, kann sogar nicht herausnehmbarer Zahnersatz (eine Brücke) eingegliedert werden. Natürlich ist auch eine Einzelzahnversorgung (1 Implantat je verlorenem Zahn) möglich, was wegen der sehr hohen Kosten aber nur in Ausnahmefällen zu verantworten ist.
-
- Ein Beispiel für eine Oberkiefer-Teilprothese (Kombinierter Zahnersatz), (hier mit 7 Doppelkronen und einem Steg auf 7 Implantaten)
Festsitzender Teil der Oberkiefer-Hybridprothese von okklusal gesehen.
Oberkiefer-Hybridprothese auf dem Arbeitsmodell von okklusal gesehen. Beachte: der harte Gaumen ist nicht mit einer Kunststoffplatte bedeckt.
Oberkiefer-Hybridprothese auf dem Arbeitsmodell von vestibulär gesehen.
-
- Ein Beispiel für eine Cover-Denture-Prothese im Unterkiefer (hier auf 4 Implantaten und 2 Stegen)
Festsitzender Teil einer Unterkiefer-Hybridprothese von vestibulär gesehen: 4 Implantate und 2 Stege
Festsitzender Teil der Unterkiefer-Hybridprothese von okklusal gesehen
Die Unterkiefer-Hybridprothese von krestal gesehen. Bei einer Vergrößerung des Bildes kann man deutlich Retentionsstifte erkennen, die der Friktion der Prothese dienen.
-
- Ein Beispiel für eine Cover-Denture-Prothese im Unterkiefer (hier auf 2 Implantaten mit Kugelköpfchen)
2 Implantate im Unterkiefer mit Patrizen zur Befestigung einer Cover-Denture-Prothese
die dazu passende Unterkiefer-Prothese mit den eingearbeiteten Matrizen
Vor- und Nachteile von Zahnimplantaten
Vorteile:
- verbesserte Kaukraft,
- verbessertes Sprechen / Phonetik,
- Verbesserung der Ästhetik,
- verringerter, oft sogar vollständiger Stopp des Knochenabbaus im zahnlosen Kieferkammbereich,
- verlängerte Verweildauer von Zahnersatz,
- verringerter Druck auf die Schleimhaut bei Teilprothesen
- Beschleifen der Nachbarzähne kann vermieden werden, also Schonung des Restzahnbestandes (besonders wichtig bei Nachbarzähnen, die noch keine oder nur kleine Füllungen haben),
- verbesserter Halt einer Prothese,
- Befestigung Totaler Prothesen als Cover-Denture-Prothese.
Nachteile bzw. mögliche Risiken:
- operativer Eingriff erforderlich,
- eventuelle Nervenverletzung (besonders des Nervus alveolaris inferior im Unterkiefer),
- da Zahnimplantate starr in den Knochen einwachsen, wird der Kaudruck nicht wie bei natürlichen Zähnen durch die Sharpey-Fasern abgefedert und kann damit zu einer Mehrbelastung des Kiefergelenks führen,
- kostenintensiv
Einzelnachweise
- ↑ Der kleine Stowasser: Lateinisch-deutsches Schulwörterbuch
- ↑ C. Mish
- ↑ Schröder, 1976, Bern
- ↑ Löffler, Petrides: Biochemie und Pathobiochemie, 7. Aufl. Springer Verl. 2003
- ↑ Helms,J.A. et al.: NATURE 423, 326-331,2003
- ↑ B.Alberts, James D. Watson et al.: Molecular Biology of The Cell, 4th Edition, Garland Science 2002.
- ↑ Zhao B, et al.: J Biol Chem, 2006
Siehe auch
Weblinks
- Risiken und Komplikationen bei Zahnimplantaten
- Neueste wissenschaftliche Veröffentlichungen
- Sendung des NDR mit vielen aufklärenden Beiträgen zum Thema Implantate "
- Arbeitsgemeinschaft Zahngesundheit - unabhängige Verbraucher- u. Patientenberatung: "Patienteninformationen zu Zahnimplantaten"
- Patienteninformationen der Mitteldeutschen Vereinigung für Zahnärztliche Implantologie e.V.
- Grenzen der Zahnimplantologie: Herz-, Kreislauferkrankungen, Blutgerinnung, Diabetes mellitus - Initiative proDente e.V.
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.