- Blei(II)-acetat
-
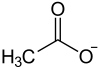
Strukturformel 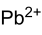
![\mathsf{ \ \!\ \Biggr]_2}](4/0f426376eaf07819e87caaef4e79bf4a.png)
Allgemeines Name Blei(II)-acetat Andere Namen - Bleiacetat
- Bleizucker
- Bleiessig
- essigsaures Blei
- essigsaures Bleioxyd (veraltet)
Summenformel C4H6O4Pb CAS-Nummer - 301-04-2 (wasserfrei)
- 6080-56-4 (Trihydrat)
Kurzbeschreibung farblose, süßlich schmeckende, monokline Kristalle[1]
Eigenschaften Molare Masse 325,28 g·mol−1 (wasserfrei) Aggregatzustand fest
Dichte Schmelzpunkt Siedepunkt Zersetzung: ab 200 °C[2]
Löslichkeit Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 

Gefahr
H- und P-Sätze H: 351-360FD-373-410 EUH: keine EUH-Sätze P: 281-273-308+313-314 [2] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 61-62-E48/22-33-50/53 S: 53-45-60-61 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Blei(II)-acetat (Pb(CH3COO)2), ein farbloser kristalliner Feststoff, ist das Blei(II)-salz der Essigsäure. Neben der wasserfreien Substanz kommt auch ein Trihydrat vor (Pb(CH3COO)2 · 3 H2O).
Inhaltsverzeichnis
Darstellung
Blei(II)-acetat kann durch Reaktion von Blei(II)-oxid mit Essigsäure gewonnen werden
Verwendung
Blei(II)-acetat dient vor allem zur Gewinnung anderer Bleiverbindungen, beispielsweise Bleichromat (Chromgelb) und basisches Bleicarbonat (Bleiweiß). Blei(II)-acetat dient auch als Nachweisreagenz für Sulfide.
Bekannt ist Blei(II)-acetat als Bleizucker, da es süß schmeckt und gut in Wasser löslich ist. Trotz seiner Giftigkeit wurde Bleizucker bis zum 19. Jahrhundert als Zuckerersatz (Defrutum) verwendet – insbesondere wurde Wein damit gesüßt. Der Komponist Ludwig van Beethoven ist wahrscheinlich an einer durch solchermaßen verpanschte Weine verursachten Bleivergiftung gestorben[4][5]. Der Begriff Bleizucker soll aus Sicherheitsgründen nicht mehr verwendet werden.
Bleipapier, ein mit einer 1%-igen wässrigen Lösung von Bleiacetat getränktes und in Schwefelwasserstoff-freier Luft getrocknetes Filterpapier,[6] dient zur qualitativen Erkennung von Schwefelwasserstoff (H2S), es entsteht braungraues, metallisch glänzendes Bleisulfid.[7]
Einzelnachweise
- ↑ Roempp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c d e f g Eintrag zu Blei(II)-acetat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26.12.2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 301-04-2 im European chemical Substances Information System ESIS
- ↑ Pharmazeutische Zeitung zu Beethovens wahrscheinlicher Bleivergiftung
- ↑ Beethoven litt unter Bleivergiftung
- ↑ Walter Wittenberger: Chemische Laboratoriumstechnik, Springer-Verlag, Wien, New York, 7. Auflage, 1973, S. 94, ISBN 3-211-81116-8.
- ↑ Römpp CD 2006, Georg Thieme Verlag 2006
Weblinks
Kategorien:- Stoff mit Verdacht auf krebserzeugende Wirkung
- Stoff mit reproduktionstoxischer Wirkung
- Umweltgefährlicher Stoff
- Stoff mit Verdacht auf reproduktionstoxische Wirkung
- Acetat
- Bleiverbindung
Wikimedia Foundation.


