- Acetoacetat
-
Strukturformel 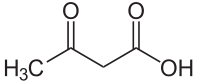
Allgemeines Name Acetessigsäure Andere Namen - 3-Oxobutansäure
- 3-Oxobuttersäure
Summenformel C4H6O3 CAS-Nummer 541-50-4 Eigenschaften Molare Masse 102,09 g·mol−1 Aggregatzustand flüssig bzw. fest[1]
Schmelzpunkt 36 - 37 °C bzw. viskose Flüssigkeit bei Raumtemperatur[1]
Siedepunkt Zersetzung
Löslichkeit mischbar mit Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung 
unbekannt R- und S-Sätze R: ? S: ? Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Acetessigsäure ist der Trivialname der 3-Oxobutansäure. Das Anion der Säure wird Acetoacetat oder auch Acetacetat genannt.
Inhaltsverzeichnis
Gewinnung und Darstellung
Acetessigsäure wird durch Verseifen (Hydrolyse) von Acetessigsäureethylester und anschließender Umsetzung mit Säuren hergestellt. Eine weitere Möglichkeit der Darstellung ist die Oxidation von Buttersäure mit Wasserstoffperoxid.
Eigenschaften
Bei Acetessigsäure liegt eine Keto-Enol-Tautomerie vor. Infolge des induktiven Effekts der Ketogruppe reagiert Acetessigsäure saurer als die ihr zugrundeliegende Buttersäure.
Verwendung
Reine Acetessigsäure wird kaum verwendet, da sie sich leicht unter Decarboxylierung in Kohlenstoffdioxid und Aceton zersetzt (schnell bei 100 °C). Wichtiger sind ihre Ester und Salze.
Biologische Bedeutung
Acetessigsäure (Acetoacetat) tritt als Zwischenprodukt im Stoffwechsel auf, zählt zu den Ketokörpern und hat besondere Bedeutung beim Katabolismus bei Hunger oder Diät. Dabei wird im Hungerzustand entstandenes Acetyl-CoA, über ein Zwischenprodukt, zu Acetoacetat umgebaut.
Einzelnachweise
Literatur
- Beilstein E III 3; 1178
Wikimedia Foundation.
