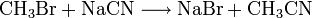- Ethylnitril
-
Strukturformel 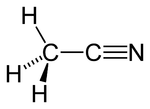
Allgemeines Name Acetonitril Andere Namen - Methylcyanid
- Ethannitril
- Azetonitril
- Essigsäurenitril
- Ethansäurenitril
- Cyanomethan
Summenformel C2H3N CAS-Nummer 75-05-8 Kurzbeschreibung farblose, leicht entzündliche Flüssigkeit mit aromatischem Geruch [1] Eigenschaften Molare Masse 41,05 g·mol−1 Aggregatzustand flüssig
Dichte 0,78 g·cm−3 [1]
Schmelzpunkt Siedepunkt 82 °C [1]
Dampfdruck Löslichkeit Mit Wasser vollständig mischbar [1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Leicht-
entzündlichGesundheits-
schädlich(F) (Xn) R- und S-Sätze R: 11-20/21/22-36 S: (1/2)-16-36/37 MAK 20 ml·m−3, 34 mg·m−3 [1]
LD50 - 2730–3800 mg·kg−1 (Ratte, oral)
- 988 mg·kg−1 (Kaninchen, dermal)
WGK 2 – wassergefährdend [1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Acetonitril ist ein organisches Lösungsmittel und gehört zur Stoffgruppe der Nitrile.
Inhaltsverzeichnis
Eigenschaften
Bei starkem Erhitzen und im Brandfall entstehen giftige Gase wie Cyanwasserstoff und Stickoxide, mit Luft entstehen explosionsfähige Gemische.
Acetonitril greift Gummi an und löst viele Polymere. Mit Säuren tritt Polymerisation ein.
Es bildet mit Wasser ein azeotropes Gemisch mit ca. 70:30 Molprozent Acetonitril zu Wasser und einem Siedepunkt von 76,5 °C, 5,5 °C unter dem Siedepunkt von reinem Acetonitril.[3]
Toxizität
Acetonitril wirkt reizend und kann ähnliche Vergiftungserscheinungen wie Blausäure (= Cyanwasserstoff) hervorrufen. Es ist gesundheitsschädlich beim Einatmen, Verschlucken und Hautkontakt. Acetonitril wird durch die Haut (perkutan) resorbiert und wirkt im Körper als Blutgift.
Verwendung
Acetonitril ist ein gebräuchliches Lösungsmittel im Labor, in der chemischen Analytik (beispielsweise HPLC) und in der technischen Chemie, dort hauptsächlich zur Extraktion von 1,3-Butadien.
Herstellung
Möglichkeiten zur Herstellung sind nucleophile Substitutionsreaktionen von z. B. Brommethan mit Natriumcyanid (NaCN).
Im folgenden Beispiel reagieren Brommethan und Natriumcyanid zu Natriumbromid und Acetonitril:
Industriell fällt Acetonitril bei der Herstellung von Polyacrylnitril in relativ geringen Mengen als Nebenprodukt an. Preis und Verfügbarkeit sind daher an die Produktion dieses Polymers gekoppelt.
Quellen
- ↑ a b c d e f g h Eintrag zu Acetonitril in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 4. Nov. 2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 75-05-8 im European chemical Substances Information System ESIS
- ↑ Ponton, Jack (September 2001). Azeotrope Databank (Queriable database). The Edinburgh Collection of Open Software for Simulation and Education, Edinburgh University. Abgerufen am 20. Februar 2008.
Weblinks
Sicherheitsdatenblätter
Wikimedia Foundation.