- Aldehyddehydrogenase 2
-
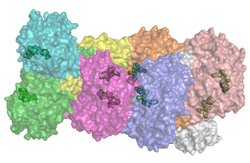
Aldehyddehydrogenase 2 Oktamer nach PDB 1CW3 Vorhandene Strukturdaten: 1a4z, 1ag8, 1cw3, 1nzw, 1nzx, 1nzz, 1o00, 1o01, 1o02, 1o04, 1o05, 1of7, 1zum, 2onm, 2onn, 2ono, 2onp Größe 500 Aminosäuren; 54,4 kDa Struktur Homotetramer Isoformen ALDH1 Bezeichner Gen-Namen ALDH2; ALDH-E2; ALDHI; ALDM; MGC1806 Externe IDs OMIM: 100650 MGI: 99600 Enzymklassifikation EC, Kategorie 1.2.1.3 Oxidoreduktasen Substrat Aldehyd + NAD+ + H2O Produkte Carbonsäure + NADH Vorkommen Übergeordnetes Taxon Lebewesen Orthologe Mensch Maus Entrez 217 11669 Ensembl ENSG00000111275 ENSMUSG00000029455 UniProt P05091 Q3TVM2 Refseq (mRNA) NM_000690 NM_009656 Refseq (Protein) NP_000681 NP_033786 Genlocus Chr 12: 110.69 - 110.73 Mb Chr 5: 121.83 - 121.85 Mb PubMed Suche [1] [2] Aldehyddehydrogenase 2 (ALDH-2) ist ein zur Gruppe der Aldehyddehydrogenasen gehörendes Enzym, welches im menschlichen Körper zum Abbau von Alkohol (Ethanol) benötigt wird. ALDH-2 wandelt das, durch ADH aus Alkohol erzeugte, toxische Acetaldehyd (Ethanal) in Acetat um.
46 Prozent der Japaner und 56 Prozent der Chinesen sind von einem Polymorphismus der Acetaldehyddehydrogenase 2 betroffen. Sie sind Träger eines dominanten Allels des ALDH2-Gens, bei dem an Position 487 der Aminosäuresequenz das Glutamat gegen Lysin ausgetauscht ist. Das mutierte ALDH2 kann Acetaldehyd weniger effektiv verarbeiten als das Wildtyp-Protein und wird selbst schneller abgebaut. [1] Dadurch kommt es leichter zu einer Anhäufung des Acetaldehyds im Körper und damit zu den mit übertriebenem Alkoholkonsum verbundenden Vergiftungserscheinungen (Flush-Syndrom). Die betroffenen Personen sind somit empfindlicher gegenüber den negativen Auswirkungen des Alkoholgenusses.
Einige Milchsäurebakterien beschreiten mit der Aldehyddehydrogenase 2 auch den entgegengesetzten Weg: Unter guten Bedingungen bauen sie das gesamte aus der Glykolyse stammende Pyruvat zu Lactat ab. Herrscht allerdings Glucosemangel, spalten verschiedene homofermentative Stämme das Pyruvat mittels Pyruvat-Formiat-Lyase außerdem in Formiat und Acetyl-Coenzym A. Die Hälfte des Acetyl-CoA kann nun von der Aldehyddehydrogenase in Acetaldehyd umgesetzt werden, das die Alkoholdehydrogenase in Ethanol umwandelt. Aus der anderen Hälfte des Acetyl-CoA wird Acetat hergestellt, das zur ATP-Synthese genutzt werden kann.
Einzelnachweise
Siehe auch
Wikimedia Foundation.