- Aldol-Reaktion
-
Eine Aldolreaktion ist eine durch Säuren oder Basen katalysierte Reaktion von Aldehyden oder Ketonen. Aldoladdition oder Aldolisation bezeichnet die Addition eines Enolats oder Enolations als Nukleophil an eine Carbonyl-Komponente als Elektrophil. Dabei entsteht ein β-Hydroxyaldehyd oder β-Hydroxyketon. Bei einer Aldolkondensation erfolgt anschließend eine Eliminierung von Wasser und es bildet sich ein α,β-ungesättigtes Carbonyl. Die Aldolspaltung oder Retroaldolreaktion ist die Rückreaktion in die Ausgangsverbindungen.
Der Name Aldehyd-Alkohol-Reaktion leitet sich vom Reaktionsprodukt, einem β-Hydroxyketon, ab.
Aldolreaktionen sind wichtige Reaktionen für die Bildung von Kohlenstoff-Kohlenstoff-Bindungen und ein grundlegendes Reaktionsprinzip in der organischen Chemie.
Inhaltsverzeichnis
Geschichte
Die Aldolreaktion wurde unabhängig voneinander von Charles Adolphe Wurtz und von Alexander Porfyrevich Borodin im Jahre 1872 entdeckt. Borodin hat hier die Dimerisierung von Acetaldehyd zu 3-Hydroxybutanal (andere Namen sind Aldol oder Acetaldol) unter sauren Bedingungen beobachtet.
Reaktion
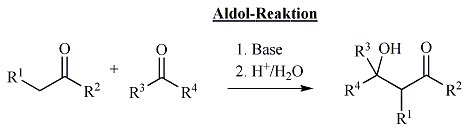
Bruttoreaktionsgleichung einer basenkatalysierten Aldolreaktion zweier Ketone (alle Reste sind Alkylgruppen) zu β-Hydroxyketon:
Sind in der obigen Reaktionsgleichung R1 bis R3 Wasserstoff und R4 eine Methylgruppe (zwei Ethanalmoleküle) entsteht das Aldol (3-Hydroxybutanal).
Im alkalischen oder auch sauren Milieu dimerisiert Ethanal (Acetaldehyd) in einer Gleichgewichtsreaktion zu 3-Hydroxybutanal. Im Sauren und/oder durch Erhitzen reagieren das gebildete Aldol unter Wasserabgabe (Dehydratisierung) weiter zum ungesättigten Aldehyd („Alkenal“), in diesem Fall Crotonaldehyd. Dieser kann als Ausgangsstoff für 1,3-Butadien (Buna-Synthese) genutzt werden.
Mechanismus
Carbonyle, die in α-Position H-Atome besitzen, werden als C,H-acide Verbindungen bezeichnet. Durch Zugabe einer Base können diese unter Bildung eines Enolats deprotoniert werden (Gleichung (1) in Bild (2)). Die Acidität hängt von verschiedenen strukturellen Faktoren ab, auch vom Energieinhalt der erzeugbaren Enolate. Ihre Ursache liegt in der Bildung eines mesomeriestabilisierten Systems begründet.
Enolate verfügen über zwei nukleophile Positionen. Mit dem Enolat-Kohlenstoff können sie andere Carbonyle am Carbonylkohlenstoff unter Bildung von β-Hydroxycarbonylen angreifen (2). Diese können schließlich thermisch bzw. basenkatalysiert zu α,β-ungesättigten Carbonylen dehydratisiert werden (3). Bei dieser Vorgehensweise spricht man von der Gesamtreaktion als Aldolkondensation. Des Weiteren ist auch ein nukleophiler Angriff des Enolat-Sauerstoffs an bestimmten Elektrophilen möglich.
Stereoselektivität
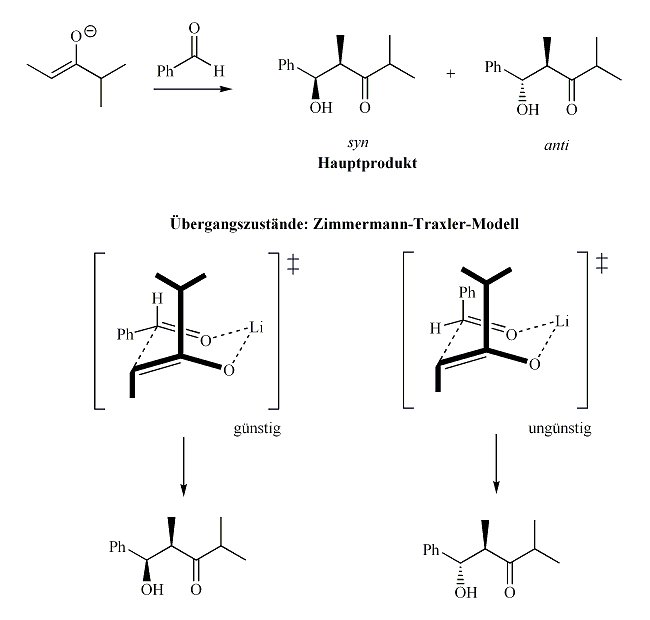
Bei der Aldoladdition kann Stereoselektivität in Form von so genannter einfacher Diastereoselektivität auftreten. Das bedeutet, dass die zwei zuvor sp2-hybridisierten Kohlenstoff-Atome (des Enolats und der Carbonyl-Komponente), die im Produkt eine gemeinsame Bindung aufweisen und jeweils ein Stereozentrum bilden, zueinander dieselbe Relativkonfiguration einnehmen. Dies wird anhand des Zimmermann-Traxler-Modells des Übergangszustands erklärt, in dem eine pseudo-Sesselkonformation angenommen wird (siehe Bild 3).
Anwendung
Die Aldolreaktion ist ein sehr weit verbreitetes Verfahren und hat seine Anwendung sowohl im Labormaßstab als auch in der großtechnischen Produktion.
Die Aldolreaktion hat in der Synthese, besonders von Naturstoffen, große Bedeutung erlangt. In engem Zusammenhang mit der Aldolreaktion stehen Namensreaktionen wie die Claisen-Kondensation, die Henry-Reaktion und die Knoevenagel-Reaktion.
Ein Schlüsselschritt in der Synthese von Atorvastatin, einem Herzmedikament von Pfizer welches 1996 eingeführt wurde, sind zwei Aldolreaktionen.
Biologische Bedeutung
Die Aldolreaktion und ihre Umkehrung sind bei vielen enzymatisch katalysierten biochemischen Reaktionen an der Veränderung des Kohlenstoffgerüstes von Naturstoffen beteiligt. Beispielsweise wird beim aeroben Kohlenhydratabbau am Anfang des Citratzyklus das Citrat aus Oxalessigsäure und Acetyl-CoA in einer Aldoladdition gebildet.
Erfolgt die Biosynthese der Isoprenoide über die Mevalonsäure, dann ist dort die Verknüpfung von Acetyl-CoA und Acetacetyl-CoA zu 3-Hydroxy-3-methylglutaryl-CoA eine Aldolreaktion.
Bei der Gluconeogenese reagieren die beiden isomeren Ketotriosen Glycerinaldehyd-3-Phosphat und Dihydroxyacetonphosphat im Sinne einer Aldolreaktion zu Fructose-1,6-bisphosphat.
Die frühere Annahme von Adolf von Baeyer und anderen, dass eine Aldolkondensation ein wichtiger Schritt der pflanzlichen Stärkesynthese ist, ist durch neuere Erkenntnisse überholt.
Literatur
- Thomas Laue, Andreas Plagens: Namen- und Schlagwort-Reaktionen der Organischen Chemie. B.G. Teubner, 1999.
- Jürgen Falbe und Manfred Regitz (Hrsg.): Römpp kompakt Basislexikon Chemie. Thieme, Stuttgart/New York 1998, ISBN 3-13-115711-9
Wikimedia Foundation.