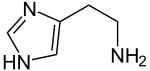
- 2-(4-Imidazoyl)-ethylamin
-
Strukturformel Allgemeines Name Histamin Andere Namen 2-(4-Imidazolyl)-ethylamin
Summenformel C5H9N3 CAS-Nummer 51-45-6 PubChem 774 ATC-Code Kurzbeschreibung Farblose Kristalle Eigenschaften Molare Masse 111,15 g·mol−1 Aggregatzustand fest
Schmelzpunkt Siedepunkt 210 °C (24 mbar)
Löslichkeit löslich in kaltem Wasser[1], Ethanol,
unlöslich in DiethyletherSicherheitshinweise Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36/37/38-42/43 S: 22-26-36/37 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 - 200 mg/kg (Meerschweinchen, oral) [2]
- 5 mg/kg (Meerschweinchen, intraperitoneal) [2]
- 220 mg/kg (Maus, oral) [3]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Histamin (histos (gr.) Gewebe, -amin stickstoffhaltige Verbindung) – in der Nomenklatur: 2-(4-Imidazolyl)-ethylamin – ist ein Naturstoff, der im menschlichen oder tierischen Organismus als Gewebshormon und Neurotransmitter wirkt und auch im Pflanzenreich und in Bakterien weit verbreitet ist. Beim Menschen und anderen Säugetieren spielt Histamin eine zentrale Rolle bei allergischen Reaktionen und ist am Immunsystem, d. h. an der Abwehr körperfremder Stoffe beteiligt. Auch im Magen-Darm-Trakt, bei der Regulation der Magensäureproduktion und der Motilität sowie im Zentralnervensystem bei der Steuerung des Schlaf-Wach-Rhythmus und der Appetitkontrolle wirkt Histamin als wichtiger Regulator. Biochemisch ist es, wie auch Tyramin, Serotonin, Dopamin, Adrenalin, Noradrenalin oder Octopamin, ein biogenes Amin. Es wird durch Decarboxylierung aus der Aminosäure Histidin gebildet und insbesondere in Mastzellen, basophilen Granulozyten und Nervenzellen gespeichert.
Inhaltsverzeichnis
Chemische Eigenschaften
Histamin bildet farblose, hygroskopische, bei 84 °C schmelzende Kristalle, die sich leicht in Wasser und Ethanol lösen, nicht jedoch in Ether. Die Verbindung liegt in wässriger Lösung als Gemisch zweier Tautomere, Nπ-H-Histamin und Nτ-H-Histamin, vor.
Histamin besitzt zwei basische Zentren, d. h. zwei Atomgruppen mit Stickstoffatomen, an die Protonen angelagert werden können. Unter physiologischen Bedingungen wird bevorzugt die aliphatische Nα-Aminogruppe mit ihrem pKa-Wert von 9,4 protoniert, während der Imidazolring (pKa = 5,8) erst in einem stärker sauren Milieu ein Proton aufnimmt.[4]
Biosynthese
Histamin wird in Mastzellen, Zellen der Epidermis und der Magenschleimhaut und in Nervenzellen synthetisiert und in Vesikeln gespeichert. In diesen Zellen wird Histamin aus der Aminosäure Histidin durch eine Pyridoxalphosphat-abhängige Decarboxylierung mittels des Enzyms Histidindecarboxylase in einer Ein-Schritt-Reaktion gebildet. In geringerem Ausmaß kann auch die unspezifische DOPA-Decarboxylase an der Biosynthese des Histamins beteiligt sein.
Abbau
Histamin wird im Körper über zwei verschiedene Wege abgebaut. Insbesondere im Zentralnervensystem erfolgt eine Inaktivierung zum Nτ-Methylhistamin durch das Enzym Histamin-N-Methyltransferase. Nτ-Methylhistamin wird nachfolgend oxidativ über Monoaminooxidasen, Diaminoxidasen und Aldehydoxidasen zur Nτ-Methylimidazolylessigsäure abgebaut[5]. In der Peripherie hingegen spielt die Histaminmethylierung eine untergeordnete Rolle. Hier erfolgt der Abbau vorwiegend über Diaminoxidasen und Aldehydoxidasen zur Imidazolylessigsäure. Diese wird nach Ribosylierung über die Nieren ausgeschieden.
Speicherung und Freisetzung
Histamin kommt in erhöhter Konzentration in den Mastzellen, den basophilen Granulozyten sowie in histaminspeichernden Zellen der Schleimhäute, der Bronchien und des Magen-Darm-Trakts vor. In diesen Zellen wird Histamin in Vesikeln an Heparin gebunden gespeichert. Aus diesen Vesikeln wird Histamin bei IgE-vermittelten allergischen Reaktionen vom „Soforttyp“ (Typ I) oder durch Komplementfaktoren (z. B. bei einem Endotoxin-bedingten Schock) freigesetzt. Neben Gewebshormonen können auch Arzneistoffe, wie beispielsweise Opiate, Muskelrelaxantien sowie Plasmaexpander und Röntgenkontrastmittel, eine Freisetzung von Histamin hervorrufen. Ein weiterer wichtiger Speicherort von Histamin sind die ECL-Zellen der Magenschleimhaut, aus denen Histamin durch Hormone und Gewebshormone, wie z. B. Gastrin, Acetylcholin und PACAP (pituitary adenylate cyclase activating polypeptide) freigesetzt werden kann.
Erhöhte Histaminkonzentrationen können auch in Teilen des Zentralnervensystems und der Gehirn-Rückenmarks-Flüssigkeit (Liquor cerebrospinalis) nachgewiesen werden. Die höchste Histaminkonzentration kann dabei im Hypothalamus gefunden werden. Innerhalb des Zentralnervensystems fungiert Histamin auch als Neurotransmitter in histaminergen Neuronen. Eine Freisetzung von Histamin in den synaptischen Spalt wird durch Acetylcholin, Noradrenalin und Histamin selbst über präsynaptische Rezeptoren gehemmt.
Funktion
Im menschlichen Organismus besitzt Histamin vielfältige Funktionen, wobei insbesondere seine Beteiligung an Abwehrreaktionen im Vordergrund steht. Auf molekularer Ebene vermittelt Histamin seine Funktionen über eine Aktivierung der Histamin-Rezeptoren H1, H2, H3 und H4, die zur Familie der G-Protein-gekoppelten Rezeptoren gehören.
Abwehrreaktionen
Wichtige Funktionen des Histamins sind seine Beteiligung an der Abwehr körperfremder Stoffe und seine pathologische Beteiligung an der Symptomatik von Allergien und Asthma. Ebenso ist Histamin eine der Mediatorsubstanzen bei Entzündungen und Verbrennungen. Hierbei führt Histamin zu Jucken, Schmerz und Kontraktion der glatten Muskulatur (beispielsweise in den Bronchien). Anders als beim Menschen spielt Histamin bei Hunden und Katzen bei der Entstehung von Juckreiz nur eine untergeordnete Rolle. Es bedingt eine erhöhte Permeabilität der Gefäßwände kleiner Blutgefäße und führt so zur Nesselsucht. An diesem Prozess ist auch eine durch Histamin induzierte Aktivierung des Transkriptionsfaktors NF-κB und eine damit verbundene vermehrte Freisetzung weiterer Entzündungsmediatoren beteiligt[6]. Histamin führt ebenfalls zu einer Freisetzung von Adrenalin aus den Nebennieren. Diese Effekte werden insbesondere über eine Aktivierung von H1-Rezeptoren vermittelt.
Histamin wirkt chemotaktisch auf verschiedene, an der Abwehr körperfremder Stoffe beteiligte Zellen, beispielsweise die eosinophilen Granulozyten und die T-Zellen. Für diese Effekte wird vor allem eine Aktivierung von H4-Rezeptoren verantwortlich gemacht[7].
Magen-Darm-Trakt
Im Magen-Darm-Trakt ist Histamin an der Regulation der Magensäureproduktion und der Motilität beteiligt. Die durch Histamin über eine Aktivierung von H2-Rezeptoren vermittelte Steigerung der Magensäureproduktion kann dabei als ein Bestandteil einer Histamin-vermittelten Abwehrreaktion interpretiert werden.
Herz-Kreislaufsystem
Ebenfalls als Bestandteil einer Abwehrreaktion kann die Wirkung von Histamin auf die Blutgefäße interpretiert werden. Es kontrahiert H1-Rezeptor-vermittelt die großen Blutgefäße (Durchmesser von mehr als 80 µm) und führt zu einer Erweiterung kleinerer Blutgefäße verbunden mit Hautrötung. Am Herzen besitzt Histamin über eine Aktivierung von H2-Rezeptoren eine positiv inotrope (die Schlagkraft steigernde) und positiv chronotrope (die Schlagfrequenz steigernde) Wirkung.
Zentralnervensystem
Im Zentralnervensystem ist Histamin über eine Aktivierung von H1-Rezeptoren an der Auslösung des Erbrechens sowie der Regulation des Schlaf-Wach-Rhythmus beteiligt. Basierend auf tierexperimentellen Befunden wird eine antidepressive, antikonvulsive und Appetit zügelnde Wirkung des Histamins diskutiert. Ebenso scheint es an der Regulation der Körpertemperatur, der zentralen Kontrolle des Blutdrucks und der Schmerzempfindung beteiligt zu sein[8]. Über präsynaptische Rezeptoren (insbesondere H3-Rezeptoren) besitzt Histamin durch Hemmung der Neurotransmitterfreisetzung im Zentralnervensystem und im peripheren Nervensystem einen regulatorischen Einfluss auf noradrenerge, serotoninerge, cholinerge, dopaminerge und glutaminerge Neuronen. Histamin beeinflusst somit indirekt die Effekte dieser Neurotransmitter.
Aktuell laufen Studien in Europa mit Histamin als Arzneistoff mit wachmachender, vigilanzsteigernder Wirkung. Zum Einsatz könnte das Medikament in einiger Zeit z.B. bei krankhaften Schlaf-Wach-Regulationsstörungen kommen.
Toxikologie
Die Verträglichkeitsgrenze von Histamin liegt bei ungefähr 10 mg. Größere Mengen Histamin führen zu einer Vergiftung, die durch akute Beschwerden wie Atemnot, Blutdruckabfall, Rötung der Haut, Nesselausschlag, Übelkeit, Erbrechen, Kopfschmerzen und Durchfall gekennzeichnet ist. 100 mg Histamin führen bereits zu deutlichen Vergiftungserscheinungen. Die Verträglichkeitsgrenze könnte bei Patienten mit einer Histamin-Intoleranz deutlich herabgesetzt sein.
Im Tierversuch zeigte Histamin bei verschiedenen Tierarten (Hund, Maus, Meerschweinchen, Ratte, Hase) negative Effekte auf Lunge und gesamtes Atmungssystem, [3][2] bei Hunden führten intravenöse Gaben von 7 mg/kg zu Störungen bei der Herzfunktion,[9] subkutane Dosen ab 28,5 mg/kg zu Durchfall und Koma.[2]
Verwendung
Histamin wird zur medizinischen Diagnostik v. a. von Atopien und Allergien eingesetzt, so im inhalativen Provokationstest und zur Positivkontrolle beim Intrakutantest. Histamin hat keine therapeutische Bedeutung. Dem gegenüber werden Arzneistoffe, welche die Freisetzung von Histamin aus Mastzellen (Mastzellenstabilisatoren) oder die Wirkung von Histamin an Histaminrezeptoren blockieren (Antihistaminika), in der Therapie verwendet. Mit Mastzellenstabilisatoren (beispielsweise Cromoglicinsäure (DNCG), Nedocromil oder Lodoxamid) und mit H1-Antihistaminika (z. B. Diphenhydramin, Loratadin oder Cetirizin) werden allergische Beschwerden symptomatisch behandelt. Darüber hinaus werden Schlafstörungen, Übelkeit und Erbrechen mit H1-Antihistaminika behandelt. H2-Antihistaminika (wie Cimetidin, Ranitidin oder Famotidin) sind als Hemmer der Magensäureproduktion bedeutende Antazida.
Ein Derivat des Histamins ist das vasodilatatorische Betahistin, welches als Antiemetikum und Antivertiginosum (also gegen Schwindel) v. a. bei Morbus Menière eingesetzt wird.
Histamin als Abwehrstoff
Histamin wird in einigen Pflanzen und Tieren auch als Abwehrsubstanz produziert und gespeichert. Beispielsweise speichert die Große Brennnessel in ihren Brennhaaren neben anderen Substanzen Histamin, das bei Berührung abgegeben wird[10]. Die Heuschrecke Poekilocerus bufonius (Pyrgomorphidae) gibt bei Gefahr ein Sekret ab, das neben Cardenoliden ca. 1 % Histamin enthält[11]. Histamin ist auch im Hautdrüsensekret der Südfrösche enthalten[12]. Darüber hinaus können tierische und pflanzliche Abwehrstoffe wie beispielsweise das Mastzelldegranulierende Peptid (MCD-Peptid) des Bienengifts Histamin aus den Mastzellen höherer Tiere freisetzen und somit eine Entzündungsreaktion auslösen[13].
Geschichte
Die Geschichte der Erforschung des Histamins begann im Jahr 1907 mit seiner Synthese als chemische Kuriosität durch die deutschen Chemiker Adolf Windaus und W. Vogt[14]. Bereits drei Jahre später (1910) gelang Henry H. Dale und G. Barger der Nachweis von Histamin im Mutterkorn und somit die Entdeckung von Histamin als Naturstoff[15]. Im gleichen Jahr wiesen Henry H. Dale und P. P. Laidlaw Histamin als körpereigene Substanz nach. Dale und Laidlaw klärten gleichzeitig einige grundlegende Funktionen des Histamins auf[16]. Die Biosynthese des Histamins aus der Aminosäure Histidin konnte durch Dankwart Ackermann ebenfalls 1910 aufgeklärt werden[17].
Daniel Bovet und A. Staub entdeckten im Jahr 1937 erste Substanzen, welche die Wirkung von Histamin hemmen (Antihistaminika)[18]. Bereits fünf Jahre später wurden mit Phenbenzamin und Mepyramin die ersten Antihistaminika in der Therapie eingesetzt. Anfang der 1950er Jahre wurden von der französischen Pharmafirma Rhône-Poulenc im Rahmen der Anti-Histaminforschung die ersten Neuroleptika entwickelt.[19] Im Jahr 1972 gelang James W. Black und Mitarbeitern die Unterscheidung zwischen H1- und H2-Rezeptoren[20]. Als weitere Subtypen des Histaminrezeptors wurden 1983 der H3-Rezeptor durch Jean-Michel Arrang mit Hilfe pharmakologischer Methoden[21] und 2000 der H4-Rezeptor durch Entschlüsselung des menschlichen Genoms[22] entdeckt.
Literatur
Quellen
- ↑ a b c Sicherheitsdatenblatt bei Merck BioSciences
- ↑ a b c d "Structure et Activite Pharmacodyanmique des Medicaments du Systeme Nerveux Vegetatif," Bovet, D., and F. Bovet-Nitti, New York, S. Karger, 1948. Vol. -, Pg. 718, 1948.
- ↑ a b Japanese Journal of Toxicology. Vol. 4, Pg. 105, 1991.
- ↑ Paiva T.B., Tominaga M. & Paiva A.C. (1970). Ionization of histamine, N-acetylhistamine, and their iodinated derivatives. J. Med. Chem., 13, 689–692.
- ↑ Schwartz J.-C., Arrang J.-M., Garbarg M., Pollard H. & Ruat M. (1991). Histaminergic transmission in the mammalian brain. Physiol. Rev. 71, 1–51. PMID 1846044
- ↑ Rihoux J.P., Michel L., Arnold R. & Konig W. (1999). Hypothetical mechanisms of action of an H1-antihistamine in asthma. Int. Arch. Allergy Immunol. 118:380-383.
- ↑ Zhang M., Venable J.D. & Thurmond R.L. (2006). The histamine H4 receptor in autoimmune disease. Expert. Opin. Investig. Drugs., 15, 1443–1452. PMID 17040202
- ↑ Pertz H.H., Elz S. & Schunack W. (2004). Structure-activity relationship of histamine H1-receptor agonists. Mini-Rev. Med. Chem. 4:935–940.
- ↑ Indian Veterinary Journal. Vol. 57, Pg. 31, 1980.
- ↑ Oliver F., Amon E.U., Breathnach A., Francis D.M., Sarathchandra P., Black A.K. & Greaves M.W. (1991). Contact urticaria due to the common stinging nettle (Urtica dioica) – histological, ultrastructural and pharmacological studies. Clin. Exp. Dermatol., 16, 1–7. PMID 2025924
- ↑ Dieter Schlee 1992, Ökologische Biochemie. Gustav Fischer, Jena 1992, S. 404f. ISBN 3-334-60393-8.
- ↑ Dieter Schlee 1992, Ökologische Biochemie. Gustav Fischer, Jena 1992, S. 421. ISBN 3-334-60393-8.
- ↑ Dieter Schlee 1992, Ökologische Biochemie. Gustav Fischer, Jena 1992, S. 409. ISBN 3-334-60393-8.
- ↑ Windaus A. & Vogt W. (1907). Synthese des Imidazoläthylamins. Chem. Berichte 40:3691.
- ↑ Barger G. & Dale, H. H. (1910). J. Chem. Soc. 97:466–473.
- ↑ Dale H.H. & Laidlaw P.P. (1910). The physiological action of β-Imidazolethylamine. J. Physiol. 41:318–344.
- ↑ Ackermann D. (1910). Z. Physiol. Chem. 60:482–501.
- ↑ Bovet D. & Staub A. (1937). Action protectrice des éthers phenoliques au cours l'intoxication histaminique. Cr. Soc. Biol. 124:547–549.
- ↑ Bangen, Hans: Geschichte der medikamentösen Therapie der Schizophrenie. Berlin 1992. S. 74–77 ISBN 3-927408-82-4
- ↑ Black J.W., Duncan W.A.M., Durant C.J., Ganellin C.R. & Parsons M.E. (1972). Definition and antagonism of histamine H2 receptors. Nature 236: 385–390.
- ↑ Arrang J.M., Garbarg M. & Schwartz J.C. (1983). Auto-inhibition of brain histamine release mediated by a novel class (H3) of histamine receptor. Nature 302: 832–837.
- ↑ Nakamura T., Itadani H., Hidaka Y., Ohta M. & Tanaka K. (2000). Molecular cloning and characterization of a new human histamine receptor, HH4R. Biochem. Biophys. Res. Commun. 279:615–620.
Weiterführende Literatur
- S. J. Hill, C. R. Ganellin, H. Timmerman, J. C. Schwartz, N. P. Shankley, J. M. Young, W. Schunack, R. Levi & H. L. Haas (1997). International Union of Pharmacology. XIII. Classification of histamine receptors. Pharmacol. Rev. 49:253–278.
- N. J. Brown & L. J. Roberts II (2001). Histamine, bradykinin, and their antagonists. In: J. G. Hardman & L. E. Limbird Goodman & Gilman's – The pharmacological basis of therapeutics, McGraw-Hill, New York, ISBN 0-07-135469-7 S.645-667.
- Dorothea M. Beutling (Hrsg.): Biogene Amine in der Ernährung, Springer, Berlin 1996, ISBN 3-540-60398-0
- H. Kasper: Ernährungsmedizin und Diätetik, Urban & Schwarzenberg, München 1996, ISBN 3-437-42011-9
- Thilo Schleip: Histamin-Intoleranz. Thrias Ehrenwirth, 2004, ISBN 3-8304-3204-6
Weblinks
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.