- 3,5-Dinitrobenzoesäure
-
Strukturformel 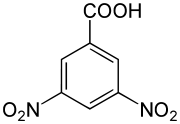
Allgemeines Name 3,5-Dinitrobenzoesäure Summenformel C7H4N2O6 CAS-Nummer 99-34-3 PubChem 7433 Kurzbeschreibung weißer bis hellgelber Feststoff[1]
Eigenschaften Molare Masse 212,12 g·mol−1 Aggregatzustand fest
Dichte 1,68 g·cm−3[1]
Schmelzpunkt pKs-Wert 2,82[3]
Löslichkeit - gut löslich in Ethanol und heißem Wasser[4]
- nahezu unlöslich in Benzol, wenig in Diethylether[4]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 
Achtung
H- und P-Sätze H: 302-315-319-335-413 EUH: keine EUH-Sätze P: 261-305+351+338 [2] EU-Gefahrstoffkennzeichnung [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36/37/38 S: 26 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Die 3,5-Dinitrobenzoesäure ist ein geruchloser, gelblicher Feststoff mit einem Schmelzpunkt von 204–206 °C. Sie gehört zur Stoffgruppe der Dinitrobenzoesäuren, die sich sowohl von der Benzoesäure als auch vom Nitrobenzol bzw. Dinitrobenzol ableitet. Die Struktur besteht aus einem Benzolring mit angefügter Carboxygruppe (–COOH) und zwei Nitrogruppen (–NO2) als Substituenten. Die 3,5-Dinitrobenzoesäure findet vor allem Verwendung in der Analyse organischer Substanzen.
Inhaltsverzeichnis
Darstellung
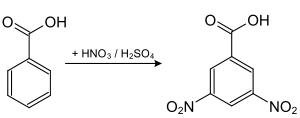
3,5-Dinitrobenzoesäure erhält man aus Benzoesäure durch Umsetzung mit rauchender Salpetersäure in Gegenwart von konzentrierter Schwefelsäure.[5][6]
Eigenschaften
Die 3,5-Dinitrobenzoesäure weist aufgrund des −M-Effekts der beiden Nitrogruppen eine höhere Acidität im Vergleich zur Benzoesäure und den Nitrobenzoesäuren auf. Der pKs-Wert ist daher entsprechend niedriger (Benzoesäure: 4,20[3]).
Verwendung
Die 3,5-Dinitrobenzoesäure findet vor allem Verwendung in der Analyse organischer Substanzen durch Derivatisierung. Flüssige Substanzen oder solche mit niedrigem Schmelzpunkt werden dazu in leicht kristallisierende Derivate umgewandelt: Alkohole können beispielsweise durch die Messung der Schmelzpunkte ihrer Ester der 4-Nitrobenzoesäure oder der 3,5-Dinitrobenzoesäure identifiziert werden. Hierzu wird die zu analysierende Substanz mit 3,5-Dinitrobenzoesäure in Gegenwart geringer Mengen Schwefelsäure umgesetzt.
-
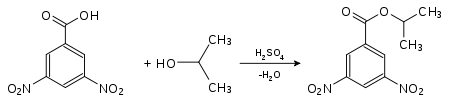 Nachweis von Isopropanol als Derivat der 3,5-Dinitrobenzoesäure:
Nachweis von Isopropanol als Derivat der 3,5-Dinitrobenzoesäure:
3,5-Dinitrobenzoesäure-2-propylester (Smp.: 123 °C[3]).
Die Schmelzpunkte dieser Derivate sind in der Regel scharf. Diese Umsetzung ist auch für zahlreiche Amine geeignet.
Die Derivate der 3,5-Dinitrobenzoesäure besitzen in der Regel höhere Schmelzpunkte als die der 4-Nitrobenzoesäure.[3] Sie werden dann bevorzugt gewählt, wenn der Schmelzpunkt mit der 4-Nitrobenzoesäure zu niedrig ist und keine genaue Bestimmung mehr möglich wird.
Ist die fragliche Substanz empfindlicher, so erfolgt stattdessen die direkte Umsetzung mit dem entsprechenden Säurechlorid, dem 3,5-Dinitrobenzoylchlorid. Auf diese Weise sind z. B. auch Derivate der Aminosäuren zugänglich.[5]
Einzelnachweise
- ↑ a b Datenblatt 3,5-Dinitrobenzoesäure bei Acros, abgerufen am 5. August 2009.
- ↑ a b c d Datenblatt 3,5-Dinitrobenzoic acid bei Sigma-Aldrich, abgerufen am 20. März 2011.
- ↑ a b c d CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ a b 3,5-Dinitrobenzoesäure. In: Römpp Chemie-Lexikon, Thieme Verlag, Stand März 2002.
- ↑ a b B. C. Saunders, G. J. Stacey, I. G. E. Wilding: „The Preparation of 3:5-Dinitrobenzoic Acid and 3:5-Dinitrobenzoyl Chloride – Observations on the Acylation of Amino-acids by means of 3:5-Dinitrobenzoyl Chloride and certain other Acid Chlorides“, in: Biochem. J., 1942, 36 (3–4), S. 368–375; PMID 16747534; PMC 1265703.
- ↑ R. Q. Brewster, Bill Williams, Ross Phillips: 3,5-Dinitrobenzoic acid. In: Organic Syntheses. Coll. Vol. 3, p. 337 (1955); Vol. 22, p. 48 (1942); PDF.
Weblinks
Wikimedia Foundation.