- Novocain
-
Strukturformel 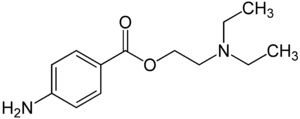
Allgemeines Freiname Procain Andere Namen 4-Aminobenzoesäure- β-diethylaminoethylester
Summenformel C13H20N2O2 CAS-Nummer - 59-46-1
- 51-05-8 (Procain-Hydrochlorid)
PubChem 4914 ATC-Code DrugBank DB00721 Arzneistoffangaben Wirkstoffklasse Wirkmechanismus Blockade spannungsabhängiger Natriumkanäle[1]
Fertigpräparate - Lophakomp-Procain (D)
- procain-loges (D)
- Procain Röwo (D)
Verschreibungspflichtig: Ja teilweise Eigenschaften Molare Masse Schmelzpunkt - 61 °C (Procain)[2]
- 153−156 °C (Procain-Hydrochlorid) [2]
pKs-Wert 8,05 bei 15 °C [3]
Löslichkeit Wasser: 9,45 g·L−1 bei 30 °C [3]
Sicherheitshinweise Gefahrstoffkennzeichnung [4]
Procain-Hydrochlorid
T
GiftigR- und S-Sätze R: 25-43 S: 24-36/37-45 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 WGK 3 (stark wassergefährdend) Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Procain ist ein Lokalanästhetikum vom Ester-Typ, das zuerst in der Zahnmedizin eingesetzt wurde. Es ist hauptsächlich unter dem Markennamen Novocain oder Novacaine bekannt.
Inhaltsverzeichnis
Geschichte
Erstmals synthetisiert wurde Procain im Jahre 1905 von dem deutschen Chemiker Alfred Einhorn, welcher dem Wirkstoff den Namen Novocain zuordnete (von lat. novus „neu“ und cain wie in Cocain). Novocain war das erste synthetische Lokalanästhetikum.
Anwendung
Procain wird für die Lokalanästhesie nur noch selten verwendet, da hierfür wirksamere, weit tiefer eindringfähige Stoffe, wie etwa Lidocain, zur Verfügung stehen. Allerdings wird es weiterhin – wegen seiner sympaticolytischen, antientzündlichen und perfusionssteigernden Wirkung – in der Neuraltherapie verwendet, einer Behandlungsform aus dem Bereich der Alternativmedizin. Relativ neu ist die Entdeckung, dass Procain das Enzym DNA-Methylase hemmen kann. Dieser Umstand kann genutzt werden, um paragenetische Schäden der Genexpression rückgängig zu machen. Dies ist vor allem bei Schäden an so genannten Tumorsuppressorgene wie p53 interessant.
Vor der Entdeckung des Procains war Cocain das meistverwendete Lokalanästhetikum. Procain besitzt keine euphorisierende Wirkung wie Cocain und fällt daher nicht unter den Geltungsbereich der Betäubungsmittelgesetze und -verordnungen.
Wirkmechanismus
Durch den Einsatz von Procain werden spannungsabhängige Natriumkanäle blockiert und somit der schnelle Natriumeinstrom (der für eine Depolarisation an der Zellmembran von Axonen zuständig ist) verhindert. Dadurch wird eine Reizweiterleitung unterbunden. In geringerem Maße werden auch andere Ionenkanäle, wie z. B. Kaliumkanäle blockiert. Damit das Lokalanästhetikum am Ionenkanal wirken kann, muss es in seiner unprotonierten Wirkform angreifen, was den Einsatz in entzündlichem Gewebe erschwert, da dort das pH-Gleichgewicht auf die Seite der protonierten Form verschoben ist.[1]
Abbau
Procain wird im Blut und in den Geweben durch die Pseudocholinesterase in Paraaminobenzoesäure (PABA) und Diethylaminoethanol verstoffwechselt.
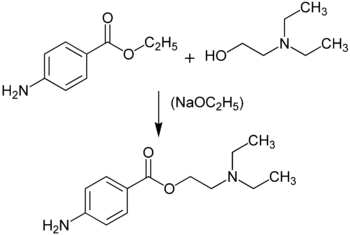
Herstellung
Es sind zwei verschiedene Methoden zur Procain-Synthese in der Literatur beschrieben.[5] Die basenkatalysierte Umesterung von 4-Aminobenzoesäureethylester mit 2-Diethylaminoethanol liefert direkt Procain:
Alternativ kann Procain aus 4-Nitrobenzoesäure hergestellt werden. Dazu wird 4-Nitrobenzoesäure mit Thionylchlorid in 4-Nitrobenzoesäurechlorid umgewandelt. Dann wird mit 2-Diethylaminoethanol verestert und die Nitrogruppe mit Wasserstoff/Raney-Nickel zur Aminogruppe reduziert.
Literatur
- Hahn-Godeffroy, J.D.: Wirkungen und Nebenwirkungen von Procain: was ist gesichert? In: Komplementäre und integrative Medizin. 02/2007, S. 32-34.
Einzelnachweise
- ↑ a b Mutschler, Geisslinger, Kroemer, Schäfer-Korting, Mutschler Arzneimittelwirkungen, 8. Auflage, 2001, ISBN 3-8047-1763-2, S. 267 ff.
- ↑ a b The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1333−1334, ISBN 978-0-911910-00-1.
- ↑ a b c Procain bei ChemIDplus
- ↑ Safety Data Sheet for PROCAINE HYDROCHLORIDE CRS – European Pharmacopoeia (Ph. Eur.) 1. September 2008
- ↑ Axel Kleemann, Jürgen Engel, Bernd Kutscher und Dietmar Reichert: Pharmaceutical Substances, 4. Auflage (2000), 2 Bände erschienen im Thieme-Verlag Stuttgart, ISBN 978-1-58890-031-9; seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen.
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.