- Transgener Mais
-
Als Transgener Mais (Genmais, Gv-Mais) werden gentechnisch veränderter Organismen des Mais bezeichnet.
In transgenen Maissorten werden bestimmte Gene aus anderen Organismen in das Mais-Genom eingeschleust, um insbesondere die Bekämpfung von Schädlingen (Bt-Mais) bzw. Unkraut (herbizidrestister Mais) zu verbessern.
Herbizidrestiste und Bt-Maissorten haben zu einer Verminderung des Einsatzes von Pflanzenschutzmitteln geführt, wodurch die Umweltbelastung durch Pestizide zurückging. Bei Bt-Mais kam es außerdem zu Ertragssteigerungen. Mit herbizidrestisten Sorten konnte die Schädlingsbekämpfung vereinfacht werden. Durch die Verwendung von transgenem Mais konnten Landwirte höhere Einkommen erzielen.[1]
Wie andere Anwendungen der Grünen Gentechnik ist auch transgener Mais in der Öffentlichkeit umstritten. Kritiker aus Umwelt- und Verbrauchergruppen und politischen Parteien sowie vereinzelte Wissenschaftler gehen von negativen ökologischen und gesundheitliche Risiken aus. Mögliche Gesundheitsrisiken sind insbesondere in der EU und in Deutschland Gegenstand jahrelanger Kontroversen. In mehreren EU-Staaten ist der Anbau von transgenem Mais verboten, nachdem sich politische Entscheidungsträger auf mögliche Umweltrisiken berufen haben.
Inhaltsverzeichnis
Gentechnische Ziele
Je nach gewünschter Eigenschaft können die Pflanzen folgende Merkmale (auch in Kombination) aufweisen:
- Resistenz gegen Breitbandherbizide (wie z.B. Roundup), um die Unkrautbekämpfung zu erleichtern.
- Insektenresistenz (z. B. gegenüber dem Maiswurzelbohrer oder Maiszünsler)
- Resistenz gegen verschiedene Schadinsekten bsp. durch Bt-Mais, der für bestimmte Insektenarten tödliche Bt-Toxine produziert und anderen transgenen Sorten wie den Avidin-Mais.
- Als erster Vertreter dieser Zielgruppe von Gv-Pflanzen überhaupt wird Trockentoleranter Mais gezüchtet.
- Das Ziel der Forschung hierbei ist zum Beispiel ein besserer Aufschluss der Maisstärke und damit mehr Effektivität bei der Herstellung von Bioethanol, auch verbesserte Futtereigenschaften.
Bt-Mais
Der Bt-Mais ist eine Variante des Gv-Mais, in die ein oder mehrere Gene des Bakteriums B. thuringiensis eingeschleust wurden. B. thuringiensis ist ein weltweit verbreitetes Bodenbakterium, dessen Unterarten über 200 verschiedene Proteine (Bt-Toxine) produzieren, die jeweils spezifisch auf die Larven bestimmter Insektenarten der Ordnungen Käfer, Schmetterlinge, Zweiflügler und Hautflügler sowie Nematoden tödlich wirken. Hierunter fallen wichtige Mais-Schädlinge wie der Maiszünsler (Ostrinia nubilalis) und der westliche Maiswurzelbohrer (Diabrotica virgifera). Die Pflanze bildet eine zunächst ungiftige Vorstufe des Toxins (Protoxin). Erst im Darm bestimmter Insekten wird es in das Protein Delta-Endotoxin umgewandelt. Nachdem es an bestimmte Rezeptoren an der Darmwand des Insekts gebunden hat, beginnt sich diese zu zersetzen, was zum Hungertod führt. Für Pflanzen, Wirbeltiere und den Menschen ist das Toxin unschädlich, da es im Magen vollständig abgebaut wird. Es ist vollständig biologisch abbaubar. Bt-Toxine werden als Präparate (Suspensionen) seit Jahrzehnten im biologischen Pflanzenschutz eingesetzt und sind auch im Ökolandbau zugelassen, zum Beispiel gegen den Maiszünsler unter dem Handelsnamen Dipel ES.[2][3]
Die konstante Präsenz des Protoxins im Feld ist der periodischen Anwendung von biologischen oder chemischen Insektiziden insofern überlegen, dass die Schadinsekten dem Gift ständig ausgesetzt sind. Ein weiterer Vorteil gegenüber der Verwendung von Bt-Suspensionen besteht darin, dass Schädlinge das Gift direkt mit ihrer Nahrung (Maispflanze) fressen, anstatt dass sie die Suspension separat aufnehmen müssen. Ein wichtiger Vorteil von Bt-Mais gegenüber konventionellem Mais in Verbindung mit chemischen Insektiziden ist die erhöhte Präzision: Schädlinge können gezielter bekämpft und Nichtzielorganismen leichter verschont werden, da diese nicht von der Pflanze fressen bzw. das Toxin bei ihnen wirkungslos ist.[3]
Aus der Perspektive des Landwirts stehen potenzielle Einsparungen bei konventionellen Insektiziden und Einkommenssteigerungen durch mögliche höhere Erträge den oft höheren Kosten des Bt-Maissaatguts im Vergleich zu konventionellem Saatgut gegenüber.
1997 kam erstmals Bt-Mais mit Resistenz gegen den Maiszünsler auf den Markt, 2003 folgte eine Variante gegen den Maiswurzelbohrer. Mittlerweile sind mehr als 100 Patente auf verschiedene gentechnische Varianten des Proteins, des Bakteriums und der veränderten Pflanzen angemeldet worden. Bekannte Anbieter von Bt-Mais sind Monsanto, Syngenta, Pioneer Hi-Bred (DuPont), Mycogen Seeds (Dow AgroSciences).
MON810
Bt-Mais der Linie MON810 des US-amerikanischen Agrarkonzerns Monsanto ist eine der am häufigsten verwendeten Sorten weltweit. Inzwischen sinkt die Verbreitung zugunsten neuerer transgener Sorten mit kombinierter Insektenresistenz und Herbizidrestistenz.[4] MON810 ist in der EU zugelassen, jedoch gibt es derzeit in mehreren europäischen Ländern Anbauverbote, darunter auch in Deutschland. In Deutschland scheiterte Monsanto im Jahr 2009 mit einer Klage gegen das vom Bundesministerium für Ernährung, Landwirtschaft und Verbraucherschutz erlassene Anbauverbot .[5] (Einzelheiten: Siehe Nationale Anbauverbote)
StarLink
StarLink war eine Bt-Maissorte von Aventis CropScience, die 1998 in den USA als Futtermitel zugelassen wurde. Als Lebensmittel war sie nicht zugelassen, da das enthaltene Cry9C-Protein Anzeichen eines Allergens hatte. Im September 2000 wurden Spuren von StarLink in Tacos sowie im Saatgut einer anderen transgenen Maissorte gefunden. Produkte wurden zurückgerufen und der Verkauf der Sorte eingestellt. Nach der Publikation der Funde in den Medien berichteten einige Verbraucher über negative Gesundheitseffekte, die in einem vermeintlichen Zusammenhang mit dem Konsum der Tacos einherging. Umfangreiche Untersuchungen durch verschiedene unabhängige Institutionen konnten jedoch keinen Zusammenhang zwischen Cry9C und diesen Fällen nachweisen.[6][7]
Trockentoleranter Mais
Bei Bakterien der Art Bacillus subtilis, die extreme Kälte überlebten, wurde ein Gen identifiziert, welches auch Pflanzen über Stresssituationen wie Trockenheit helfen kann. In Feldversuchen erzielte der mit diesem cspB-Gen ausgestattete, trockenresistente Mais von BASF und Monsanto eine Ertragssteigerung von sechs bis zehn Prozent. Die Produktzulassungen sind bei den entsprechenden Behörden in Nordamerika, Kolumbien und in der Europäischen Union beantragt. [8]
Phytase-Mais
Die chinesischen Behörden erteilten 2009 Phytase-Mais die Zulassung zum Anbau. Phytase-Mais wurde von chinesischen Forschungseinrichtungen entwickelt und bildet infolge eines eingeführten Gens das Enzym Phytase, wodurch Schweine und Geflügel den im Maisfutter enthaltenen Phosphoranteil verwerten können. Zugleich sinkt die Umweltbelastung, da Gülle und Stalldung weniger mit Phosphaten belastet sind. Mit großflächigem Anbau wird 2011 oder 2012 gerechnet.[9]
Avidin-Mais
Mit dem Avidin-Mais wurde im Labor ein transgener Mais entwickelt, der in der Lage ist, das Hühnereiprotein Avidin in Konzentrationen über 100 ppm zu exprimieren. Dieses schützt den Mais aufgrund der Biotin-Bindung vor allem bei der Lagerung gegen Schädlingsbefall, da es verhindert, dass die Schadinsekten dieses aufnehmen können.[10] Auf diese Weise sollen Ernteausfälle durch Insektenbefall während der Lagerung vor allem in tropischen Ländern reduziert werden.[11] Zudem wurden Experimente durchgeführt, wie Synergieeffekte von Bt- und Avidin-Mais als Insektenschutz genutzt werden können.[12]
Die geringere Biotin-Verfügbarkeit durch den erhöhten Avidin-Gehalt ist jedoch ein Problem für die Verwendung bei Nahrungspflanzen. Avidin verliert seine biotinbindende Wirkung nur, wenn es gekocht wird. Die FDA verbietet die Nutzung von Nahrungsmitteln, in denen der Gehalt einzelner Nährstoffe reduziert ist. Wissenschaftler empfehlen daher, die Avidin-Strategie zunächst nur bei Nichtnahrungspflanzen, wie Baumwolle, Rasengräsern, Bäumen sowie Zier- und Energiepflanzen einzusetzen. Von aktuellen Weiterentwicklungen beim Mais ist nichts bekannt.[11][13][14]
Amylase-Mais
Mais wird zunehmend für die Herstellung von Ethanol angebaut (in den USA auf ca. 40 % der Maisanbaufläche). Die pflanzliche Stärke wird mit Hilfe von Amylase-Enzymen in Zucker umgewandelt, aus welchem durch Hefegärung der gewünschte Alkohol entsteht. Die natürlicherweise im Mais vorkommenden Amylasen sind nicht ausreichend hitzestabil. In den USA wurde 2011 eine Sorte zugelassen, welche die bisher erforderliche Zugabe der Enzyme überflüssig macht, wodurch Produktionskosten sinken und sich der Wirkungsgrad verbessert.[15][16]
Anbau
Gv-Mais war einer der ersten GVO, die wirtschaftlich im großen Stil angebaut und als Nahrungspflanzen genutzt wurden. Die Anbaufelder liegen vor allem in den USA, wo im Jahr 2000 bereits über zehn Millionen Hektar angepflanzt waren. 2009 erfolgt der Anbau dort auf einer Fläche von 29,9 Millionen Hektar, was einem Anteil von rund 85% entspricht. Dabei entfallen 17% auf insektenresistente, 22% auf herbizidresistente Sorten und 46% auf eine Kombination aus beidem.[4] Für Bt-Mais bestehen bestimmte Anbauregeln in den USA, die Resistenzentwicklungen bei Fraßinsekten vermeiden sollen. Demnach müssen 20% der Fläche (in einigen Gegenden im Süden 50%) als Rückzugsgebiete mit für die Insekten unschädlichen Sorten angebaut werden.[17]
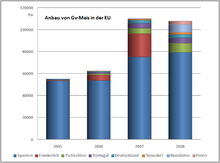
Ein Pilotprojekt in Deutschland startete 1998 mit der Aussaat auf 350 Hektar im Rahmen der Sortenprüfung. In der EU-27 wurden 2009 zusammen etwa 95.000 Hektar Gv-Mais angepflanzt, davon 80% in Spanien (22% der spanischen Maisanbaufläche).[18]
Weltweit fand der Anbau von GVO 2009 auf 134 Millionen Hektar statt (davon 42 Millionen Hektar transgener Mais, wobei Bt-Mais den größten Teil ausmacht). Das entspricht dem 7,1-fachen der gesamten deutschen Landwirtschaftsfläche (18,8 Millionen Hektar [2008])[19] bzw. 9% des weltweit nutzbaren Ackerlandes (1,5 Milliarden Hektar).[20] Transgener Mais wurde 2009 in den USA, Argentinien, Brasilien, Kanada, Südafrika, Uruguay, den Philippinen, Spanien, Chile, Honduras, Tschechien, Rumänien, Portugal, Polen, der Slowakei und Ägypten angebaut. In Deutschland wurde nur bis 2008 transgener Mais angebaut, 2009 nicht mehr.[18]
Richtlinien für die Zulassung
In vielen Ländern erfolgen die Zulassung zum Anbau und die Zulassung als Lebens- und Futtermittel getrennt voneinander. Es gibt mit Stand Juli 2011 Zulassungen für den Anbau und als Lebens- und Futtermittel in der EU und in 19 weiteren Ländern. Lediglich als Futter- und Lebensmittel sind außerhalb der EU in 11 Staaten Gv-Maislinien zugelassen.[21]
Europa
Außerhalb der EU sind Gv-Maislinien in Russland und der Schweiz als Lebens- und Futtermittel zugelassen.[21]
Europäische Union
In der EU ist die Zulassung von Gv-Pflanzen als Futter- und Lebensmittel von der Zulassung zum Anbau getrennt geregelt. Die Verordnung 1829/2003 regelt die Zulassung als Lebens- und Futtermittel und die Richtlinie 2001/18/EG (Freisetzungsrichtlinie) die Zulassung zum Anbau. 2011 sind in der EU 24 Sorten als Futter- und Lebensmittel zugelassen, davon 2 auch für den Anbau (MON810, T25). Anträge über weitere 14 Sorten für den Anbau und über 20 als Futter- und Lebensmittel sind in Bearbeitung.[22]
Auf Grund der noch herrschenden Rechtsunsicherheit bei GVO-Beimischungen kommt es immer wieder zu Berichten in den Medien, weil Behörden auf geringfügige Anteile von GVO-Saatgut in konventionellen Chargen uneinheitlich reagieren. 2009 und 2010 wurden nach Angaben der Behörden geringfügige, an der Nachweisgrenze befindliche Spuren (0,1 %) der Linie NK603 gefunden, die zwar als Lebens- und Futtermittel zugelassen ist, aber nicht zum Anbau.[23][24]
Nationale Anbauverbote
Auf Basis der in der Freisetzungsrichtlinie enthaltenen Schutzklausel (Artikel 23 2001/18/EG) ist in mehreren EU-Ländern (Deutschland, Österreich, Frankreich, Ungarn, Luxemburg und Griechenland) der Anbau von MON810 verboten.[25]
Zu Beginn des Jahres 2000 wurde der Anbau in Deutschland durch die damaligen Grünen-Minister Jürgen Trittin und Andrea Fischer gestoppt. Im Zuge von Gesetzesänderungen wurde ab 2004 zunächst der Erprobungsanbau wieder aufgenommen. Durch Übernahme der EU-Freisetzungsrichtlinie in nationales Recht konnte ab 2006 auch kommerzieller Anbau erfolgen.
Im März 2009 entschieden die EU-Umweltminister, dass die Anbauverbote von Österreich und Ungarn nicht aufgehoben werden sollen. Die EU-Kommission hatte zuvor vorgeschlagen, die nationalen Anbauverbote aufzuheben, nachdem eine erneute Sicherheitsüberprüfung für MON810 und T25 keine neuen wissenschaftlichen Erkenntnisse über schädliche oder unerwünschte Auswirkungen als Folge eines Anbaus der beiden gv-Maislinien gefunden hatte.[26]
Am 14. April 2009 setzte CSU-Landwirtschaftsministerin Ilse Aigner die Anbaugenehmigung für MON810 unter Berufung auf die Schutzklausel der Freisetzungsrichtlinie (Artikel 23 2001/18/EG) aus und sagte, „dass es berechtigten Grund zu der Annahme gibt, dass der genetisch veränderte Mais der Linie MON810 eine Gefahr für die Umwelt darstellt“.[27][28] Zehn deutsche Wissenschaftsorganisationen (unter anderem Helmholtz-Gemeinschaft, Fraunhofer-Gesellschaft, Max-Planck-Gesellschaft, Deutsche Forschungsgemeinschaft, Leibniz-Gemeinschaft) kritisierten in einer gemeinsamen Erklärung die Entscheidung, unter anderem mit der Begründung, dass eine pauschale Ablehnung der Grünen Gentechnik dem Forschungsstandort Deutschland nachhaltig schade.[29] Im Mai 2009 wurde die Anordnung der Landwirtschaftsministerin im Hauptverfahren nach einer Klage der Firma Monsanto vom niedersächsischen Oberverwaltungsgericht bestätigt.[30] Am 7. Juli 2009 veröffentlichte die Zentrale Kommission für die Biologische Sicherheit (ZKBS) beim Bundesamt für Verbraucherschutz und Lebensmittelsicherheit (BVL) eine Stellungnahme zur Risikobewertung von MON810. Dabei wurde festgestellt, „dass vom Anbau von MON810 keine schädlichen Auswirkungen auf die Umwelt ausgehen“. Die Studien, welche zum Teil maßgeblich herangezogen wurden für das Anbauverbot, umfassten zumeist Laboruntersuchungen und nicht die Situation unter Anbaubedingungen.[31][32] Zuvor hatten französische Forscher eine Auswertung von wissenschaftlicher Literatur (376 Publikationen) zu Bt-Mais seit 1996 vorgenommen und waren zu dem Schluss gekommen, dass es keine wissenschaftliche Grundlage für ein Anbauverbot gebe.[33][34]
Am 8. September 2011 urteilte der EuGH, dass sich das französische Anbauverbot von MON810 von 2008 auf die Freisetzungsrichtlinie 2001/18/EG (Artikel 23) berief, obwohl Verordnungen 1829/2003 und 178/2002 zuständig waren. Die Richtlinie 2001/18/EG erlaubt den Erlass derartiger Maßnahmen aus eigener Initiative und unmittelbar. Unter den Verordnungen 1829/2003 und 178/2002 ist der Erlass solcher Sofortmaßnahmen durch einen Mitgliedstaat nur erlaubt, wenn dieser die Kommission offiziell von der Notwendigkeit in Kenntnis setzt, Sofortmaßnahmen zu ergreifen, und die Kommission keine Maßnahme ergriffen hat. Im Rahmen der Verordnung 1829/2003 dürfen EU-Mitgliedsstaaten EU-weit zugelassene Gv-Pflanzen nur verbieten, wenn sie außer der Dringlichkeit das Vorliegen einer Situation begründen, „in der ein erhebliches Risiko bestehen kann, das offensichtlich die Gesundheit von Mensch oder Tier oder die Umwelt gefährdet“.[35]
Kennzeichnungspflicht
In der EU muss gentechnisch veränderter Mais in Lebensmitteln kenntlich gemacht werden, beispielsweise mit dem Hinweis genetisch veränderter Mais oder aus genetisch verändertem Mais[36]. Chemisch modifizierte Lebensmittelzusatzstoffe (Zusatzstoffe der zweiten Generation) aus gentechnisch verändertem Mais, wie etwa modifizierte Maisstärke, müssen nicht gesondert gekennzeichnet werden. Nicht ausgezeichnet werden bisher zudem tierische Produkte, die durch Verfütterung von gentechnisch verändertem Mais gewonnen werden. Dieser kann seit August 2005 zu diesem Zwecke in der EU importiert werden.
Honig mit Spuren von gentechnisch verändertem Mais
Der Kaisheimer Hobby-Imker Karl Heinz Bablok hatte 2005 DNA von MON810 und genetisch veränderte Proteine im Maispollen in seinen Bienenstöcken sowie DNA von MON810 in seinem Honig gefunden. Da er den Honig nicht mehr für verkehrs- und gebrauchsfähig hielt, verklagte er den Freistaat Bayern, welcher MON810 zu Forschungszwecken in einer Entfernung von etwa 500 Metern von Babloks Grundstücken anbaute, auf Schadensersatz. Im Mai 2007 verpflichtete daraufhin das Verwaltungsgericht Augsburg den Betreiber einer der Äcker, MON810 am Blühen zu hindern – durch frühzeitige Ernte oder Abschneiden der einzelnen Blütenstände. Nur so könne verhindert werden, dass Bienenvölker in der Nähe des Maisackers auch transgene Maispollen einsammeln. Honig, der MON810-Pollen enthält, sei nicht als Lebensmittel zugelassen, argumentierte das Gericht. Einen Monat später wurde dieser Entscheid zunächst durch das Bayerische Verwaltungsgericht[37] aufgehoben. Im September 2011 entschied der Europäische Gerichtshof (EuGH), dass Pollen von Gv-Pflanzen nicht als GVO und Honig mit Pollengehalt von Gv-Pflanzen als Produkt mit Zutaten aus GVO anzusehen sind, und dass Honig mit Gv-Spuren im Pollen unter die Verordnung 1829/2003 fällt. Damit widerspricht der EuGH der bisherigen Rechtspraxis, nach der Pollen als natürlicher Bestandteil des Honigs angesehen wurde und damit irrelevant war, ob Gv-Spuren im Pollen waren. Honig galt außerdem bisher als tierisches Produkt (was nicht unter die Verordnung 1829/2003 fällt). Durch das Urteil muss die Honigzutat Pollen gekennzeichnet werden, wenn der Anteil von Pollen aus zugelassenen Gv-Pflanzen mehr als 0,9% am Gesamtpollengehalt beträgt. Für Honig und Nahrungsergänzungsmittel, die Pollen aus nicht zugelassenen Gv-Pflanzen enthalten gilt ebenso wie für nicht zugelassene GVO ein Verbot des Inverkehrbringen. MON810 ist nicht unter 1829/2003 zugelassen, sondern unter der alten Verordnung 90/220; damit ist Honig mit Spuren von MON810 im Pollen ebenfalls nicht verkehrsfähig, obwohl er als Futter- und Lebensmittel unter 90/220 zugelassen ist. Das Urteil hat auch Auswirkungen auf importierten Honig aus Ländern Nord- und Südamerikas, in denen Gv-Pflanzen angebaut werden, die teilweise in der EU nicht als Futter- und Lebensmittel zugelassen sind. Weitreichende Folgen könnte das Urteil auch für Freisetzungen zu Forschungszwecken mit Gv-Pflanzen haben. Sollte die Möglichkeit, dass einzelne gv-Pollenkörner in Honig oder Spuren von gentechnisch verändertem Saatgut und gentechnisch veränderte Proteine in Pollen gelangen könnten, ausreichen, um gegen die Betreiber von Freilandversuchen gerichtlich vorzugehen, könnten Freilandversuche nicht mehr möglich sein.[38][39][40][41][42]
Naturschutzgebiete in Deutschland
In Naturschutzgebieten, in denen die Ausbringung von Bioziden untersagt ist, kann die Naturschutzbehörde den Anbau untersagen. Ein entsprechendes Urteil erließ im Jahr 2007 das Verwaltungsgericht Frankfurt an der Oder.[43] Danach ist der Anbau von Bt-Mais mit der im NSG verbotenen Ausbringung von Bioziden gleichzusetzen.
Nord- und Südamerika
Zum Anbau und als Lebens- und Futtermittel gibt es Zulassungen für transgene Maislinien in Kanada, den USA, Brasilien, Argentinien, Kolumbien und Uruguay. Darüber hinaus gibt es Zulassungen als Lebens- und Futtermittel in Mexiko und El Salvador.[21]
Afrika
Zum Anbau und als Lebens- und Futtermittel gibt es in Afrika Zulassungen für transgene Maislinien in Südafrika und Ägypten. Kenia erlaubte anlässlich der Hungerkrise am Horn von Afrika 2011 den Import für die Verarbeitung zu Maismehl.[21]
Asien
Transgene Maislinien sind zum Anbau und als Futter- und Lebensmittel in Japan, Korea und auf den Philippinen zugelassen. Lediglich als Futter- und Lebensmittel gibt es daneben Zulassungen in Taiwan, China und Singapur.[21]
Ozeanien
Als Futter- und Lebensmittel sind transgene Linien erlaubt in Australien.[21]
Erfahrungen mit transgenem Mais
Herbizidrestister Mais
In den meisten Fällen wurden keine Ertragsvorteile gegenüber konventionellem Mais beobachtet. Jedoch zeigen sich in Studien für die USA, Kanada, Südafrika und Argentinien Kosteneinsparungen durch geringeren Einsatz von Herbiziden, Arbeit und Maschinen, die die höheren Saatgutkosten mehr als aufwiegen. Herbizidrestister Mais steigerte in allen untersuchten Ländern Deckungsbeiträge und Farmeinkommen.[1]
Umweltwirkung
Der geringere Einsatz von Herbiziden wirkt sich positiv auf die Umwelt aus: Die Umweltbelastung durch Herbizide bei Einsatz von herbizidrestistem Mais, gemessen im Environmental Impact Quotient (EIQ), lag 2005 in den USA um 4%, in Kanada 5% und in Südafrika um 0.44% unter dem Wert für konventionellen Mais.[1] Im Zeitraum 1996-2008 wurden beim Anbau herbizidrestister Maissorten geschätzte 111 Millionen kg insbesondere stark toxischer Herbizide eingespart, was einer Reduktion der Umweltbelastung durch Pestizide von 8,5 % entspricht.[44]
Die Literaturstudie "Ökologische Effekte von gentechnisch verändertem Mais mit Insektenresistenz und/oder Herbizidresistenz" vorgestellt vom Bundesministerium für Gesundheit und Frauen, durchgeführt von Mag. Marion Dolezel, Dr. Andreas Heissenberger und Dr. Helmut Gaugitsch kommt bei herbizidrestisten Mais zu folgenden Ergebnissen: Bezogen auf die Britischen "Farm Scale Evaluations" zeigte sich, dass, wenn in die Studie Felder mit Einsatz von Atrazin im Vorauflauf nicht einbezogen wurden, der Unterschied in der Biodiversität von Beikräutern und Arthropoden zwischen herbizidrestisten und konventionellen Maisfeldern geringer ausfiel als in der ursprünglichen Untersuchung. Die Biodiversität in den Feldern mit herbizidrestistem Mais war hier dennoch geringfügig höher als bei konventionell bewirtschafteten Maisfeldern. Andere Studien zeigten, dass die dauerhafte Anwendung eines Totalherbizids wie beispielsweise Glyphosat Änderungen in Beikrautgesellschaften zur Folge haben kann. Es wird vermutet, dass die großflächige Anwendung von Totalherbiziden verstärkt Infektionen der Pflanzen mit Wurzelpathogenen verursacht. Der Grund hierfür wird in einer verzögerten Herbizidaufnahme gesehen. Seit herbizidrestiste Kulturpflanzen intensiv zum Einsatz kamen, wurden ebenfalls herbizidrestiste Beikräuter festgestellt. Es wird vermutet, dass die Zahl herbizidrestister Beikräuter bezüglich Häufigkeit und Frequenz weiter ansteigen wird.[45][46]
Bt-Mais
Durch die verbesserte Schädlingskontrolle führte der Bt-Mais zu Ertragsvorteilen von mehr als 5% in den USA, Kanada und Spanien. In Argentinien werden die Ertragszuwächse auf 9% geschätzt. Auf den Philippinen wurden Ertragszuwächse von 24.5% plus eine Qualitätsverbesserung von 10% festgestellt. Die Kosteneinsparungen durch geringere Anwendung von Insektiziden sind höher als der Kostenanstieg beim Saatgut. Bt-Mais steigerte in allen untersuchten Ländern Deckungsbeiträge und Farmeinkommen.[1][47][48]
Längerfristige Beobachtungen von Schädlingspopulationen in den USA haben ergeben, dass die Verwendung von Bt-Pflanzen nicht nur zu einem geringeren Schädlingsbefall in den Bt-Feldern, sondern auch zu einem geringeren Schädlingsbefall in konventionellen Feldern geführt hat (Positive Externalität).[49] US-amerikanische Maisbauern, die keinen Bt-Mais anbauten, haben auf diese Weise massiv vom Anbau des Bt-Mais durch andere Bauern profitiert.[50]
Neben dem internen Schutz der Pflanzen vor spezifischen Schädlingen haben Studien in mehreren Ländern ergeben, dass der Bt-Mais weit weniger mit Schimmelpilzen und den zugehörigen, meist krebserregenden Giften der Pilze belastet ist. Dies liegt an der verringerten Fraßschädigung, die zugleich ein Ansammeln von Wasser in den Fraßgängen und damit ein Wachstum der Pilze verhindert.[51][52]
Umweltwirkung
Der geringere Einsatz von Insektiziden wirkt sich positiv auf die Umwelt aus: Die Umweltbelastung von Pestiziden durch Bt-Mais, gemessen im EIQ, lag 2005 in den USA um 5%, in Südafrika um 2% und in Spanien um 30% unter dem Wert für konventionellen Mais.[1] Im Zeitraum 1996-2008 wurden durch den Anbau von insektenresistenten Maissorten knapp 30 Millionen kg Insektizide eingespart, was einer Reduktion der Umweltbelastung durch Pestizide von 30 % entspricht.[44]
Über die Wurzel gibt Bt-Mais Bt-Toxine an den Boden ab. Die Forscher TAPP & STOTZKY (1995) zeigten, dass cryIIIA-Proteine sich an Tonmineralen im Boden anreichern. Dadurch dass die Tonpartikel die Toxinproteine adsorbieren und binden, sind die Toxine mehrere Monate stabil. Die insektizide Wirkung bleibt bis zu 234 Tagen bestehen. Es liegen noch wenig Kenntnisse über die Ausirkung hiervon vor[53].
In einem Monitoring des spanischen Umweltministeriums über 12 Jahre konnten keine negativen Auswirkungen auf Nichtzielorganismen oder die Umwelt festgestellt werden.[54]
Resistenzbildung
Um die Resistenzbildung von Schädlingen gegen Bt-Toxine zu erschweren, ist es beim Anbau in den USA vorgeschrieben, einen kleinen Teil des Felds mit konventionellem Saatgut auszusäen. Resistenzen werden wahrscheinlich rezessiv vererbt.[55] Des Weiteren wurden bereits transgene Maissorten mit mehreren Bt-Genen entwickelt, um die Resistenzentwicklung zu erschweren.
Bisher sind die meisten Schadinsekten anfällig für die Toxine der bisher kommerzialisierten Sorten Bt-Mais. In Einzelfällen bildeten sich jedoch Resistenzen. Auf Puerto Rico wurden 2006 Resistenzen von Spodoptera frugiperda gegen Cry1F beobachtet, die zu Ernteverlusten geführt hatten. Die wahrscheinlichen Ursachen sind eine mögliche nichtrezessive Vererbung der Resistenz sowie schnellere Generationenfolge der Insekten. Die Bt-Maissorte wurde vom Markt genommen. In Südafrika wurden Resistenzen von Busseola fusca gegen Cry1Ab festgestellt. Im Sommer 2009 wurden in Bt-Maisfeldern mit Fraßschäden in Iowa Exemplare des westlichen Maiswurzelbohrers gefunden, die gegen Cry3Bb1 resistent geworden waren. Die wahrscheinlichen Ursachen sind eine unzureichende Einhaltung der Refugienflächen und eine mögliche nichtrezessive Vererbung der Resistenz.[56][57]
Sicherheit als Lebens- und Futtermittel
Wie andere transgene Pflanzen werden auch transgene Maissorten nur als Lebens- bzw. Futtermittel zugelassen, wenn anhand umfangreicher Untersuchungen gezeigt wurde, dass sie gesundheitlich ebenso unbedenklich ist wie die entsprechenden konventionellen Maissorten. So sind vergleichende Analysen der nutritiven, anti-nutritiven, toxischen und allergenen Inhaltsstoffe durchzuführen, um mögliche, durch die genetische Modifikation ausgelöste unbeabsichtigte Veränderungen feststellen zu können. Aktuelle Leitlinien für die Sicherheitsbewertung genetisch veränderter Pflanzen und daraus hergestellter Lebensmittel wurden 2004 von der Europäischen Behörde für Lebensmittelsicherheit (EFSA) und der für internationale Lebensmittelstandards zuständigen Codex Alimentarius Kommission im Juni 2003 herausgegeben. Sie basieren auf dem von einer Arbeitsgruppe der OECD im Jahr 1993 beschriebenen und von FAO und WHO in den folgenden Jahren weiterentwickelten Prinzip der Substanziellen Äquivalenz. In Deutschland ist das Bundesamt für Verbraucherschutz und Lebensmittelsicherheit im Benehmen mit dem Robert Koch-Institut und dem Bundesinstitut für Risikobewertung (BfR) für die Sicherheitsbewertung genetisch veränderter Lebens- und Futtermittel zuständig.[58]
Key u. a. (2002) verweisen darauf, dass Gentechnisch veränderte Lebensmittel (Gv-Lebensmittel) seit mehr als 15 Jahren von Hunderten Millionen Menschen weltweit konsumiert werden, ohne dass ein negativer Gesundheitseffekt bekannt sei.[59]
Unerwartete und unbeabsichtigte Veränderungen der Zusammensetzung von Organismen treten laut einer gemeinsamen Veröffentlichung des Institute of Medicine und des National Research Council (2004) bei allen Formen der genetischer Modifikation auf, inklusive gentechnischer. Ob derartige Veränderungen zu Gesundheitseffekten führen, hänge von der Natur der veränderten Substanzen und ihren biologischen Konsequenzen ab. Bisher seien keine negativen Gesundheitseffekte bei Menschen dokumentiert, die auf Gentechnik zurückgehen.[60]
Die British Medical Association (2004) und die The Royal Society (2002) schlossen in ihren Reviews, dass es keine robusten Hinweise gebe, dass Gv-Lebensmittel unsicher seien, fordern aber weitere Forschung und Beobachtung.[61]
Der Union der deutschen Akademien der Wissenschaften (2004) zufolge stellen Lebensmittel aus transgenen Pflanzen kein Risiko dar. Transgener Mais sei mehreren Untersuchungen zufolge aufgrund einer geringeren Kontamination mit Fusarium grundsätzlich gesünder als konventioneller Mais.[62]
König u. a. (2004) schreiben, dass es keine Hinweise auf mögliche negative Effekte durch den Konsum transgener Pflanzen gebe. Alle zugelassenen transgenen Pflanzen seien auf Einzelfallbasis umfangreich getestet worden.[63]
Laut einem Review von Aumaitre (2004) wurden bei bis September 2003 veröffentlichten Fütterungsstudien mit als Futtermittel zugelassenen transgenen Maissorten keine toxischen oder sonstigen negativen Effekte gefunden.[64]
Flachowsky u. a. (2005) fassen in einem Review zusammen, dass viele Studien durchgeführt worden seien und diese keine signifikanten Unterschiede zwischen den bisher kommerzialisierten transgenen und konventionellen Pflanzen im Hinblick auf Sicherheit oder Nährwert von aus ihnen hergestellten Futtermitteln festgestellt hätten.[65]
Einer 2005 veröffentlichten Studie der WHO zufolge haben die auf dem internationalen Markt gehandelten Gv-Lebensmittel Risikountersuchungen in mehreren Ländern durchlaufen. Es sei nicht wahrscheinlich und wurde bisher nicht gezeigt, dass diese Lebensmittel Risiken für die menschliche Gesundheit darstellen.[66]
Domingo (2007) fand, dass die bis dato in Fachzeitschriften veröffentlichten Sicherheitsstudien mit transgenen Maissorten keine signifikanten Unterschiede zu konventionellen Sorten gefunden hätten. Die Zahl der veröffentlichten Studien sei jedoch sehr gering. Domingo forderte weitere und längere Untersuchungen und stellte das Prinzip der Substanziellen Äquivalenz in Frage.[67]
Eine vom Gremium für genetisch veränderte Organismen der ESFA beauftragte Arbeitsgruppe zur Fütterungsstudien zur Sicherheit von transgenen Pflanzen als Futter- und Lebensmittel kam in ihrem 2008 veröffentlichten Review zu dem Schluss, dass viele subchronischen Fütterungsstudien mit transgenen Pflanzen an Nagetieren in den letzten 15 Jahren durchgeführt wurden. Diese Studien entsprächen international akzeptierten Vorgehensweisen und gaben keine Hinweise auf irgendwelche negativen Effekte. Zahlreiche Viehfütterungsstudien hätten zudem gezeigt, dass sich auf transgenen und konventionellen Pflanzen basierende Futtermitell im Hinblick auf Nährstoffaufnahme, Gesundheit und Leistung, Bruterfolg, Milchertrag und -qualität sowie anderen Indikatoren nicht voneinander unterscheiden.[68]
Querci u. a. (2008) vom Institut für Gesundheit und Verbraucherschutz (IHCP) der Gemeinsamen Forschungsstelle glauben, dass es bereits umfangreiches gesammeltes Wissen zu Sicherheitsfragen um gentechnisch veränderte Produkte gebe und dass dieses Wissen ausreiche, um die Sicherheit derzeitiger Produkte zu evaluieren. Es lägen keinerlei Berichte über Beweise irgendwelcher Gesundheitseffekte von bisher in den Zulassungsprozess eingereicheten gentechnisch veränderten Lebensmitteln vor. Gleichzeitig wisse man wenig über die Langzeitfolgen von Lebensmitteln allgemein. Die Sicherheit gentechnisch veränderter Lebensmittel ist dabei nicht absolut, sondern im Vergleich zu konventionellen Äquivalenten. Konventionelle Lebensmittel werden oft auf Basis des sicheren Konsums in der Vergangenheit evaluiert. Die gegenwärtige Erfahrung mit Langzeituntersuchungen im Rahmen von Zulassungsprozessen wiesen mit einem angemessenen Grad von Gewissheit auf einen Mangel an möglichen Gesundheitsfolgen gentechnisch veränderte Produkte hin.[69]
Lemaux (2008) kommt in ihrem Review zu dem Schluss, dass es keine wissenschaftlich validen Hinweise gebe, dass sich Gv-Lebensmittel hinsichtlich Lebensmittelsicherheit von konventionellen unterscheiden.[70]
Magaña-Gómez und Calderón de la Barca (2009) fanden in den meisten der zwischen 1998 und 2007 veröffentlichten Sicherheitsstudien mit transgenen Maissorten keine signifikanten Unterschiede zu konventionellen Maissorten, bei vier Studien seien hingegen Abweichungen festgestellt worden. Sie fordern eine stärkere Systematisierung der Sicherheitsforschung. Aufgrund der unterschiedlichen Resultate verschiedener Untersuchungen seien mehr wissenschaftliche Anstrengungen notwendig, um mehr Vertrauen in die Sicherheitsforschung und Akzeptanz von gentechnisch veränderten Lebensmitteln zu erreichen.[71]
Ein 2001 veröffentlichtes Review der Europäischen Kommission von 81 Studien aus 15 Jahren fand keine Hinweise auf Gesundheitsrisiken durch transgene Pflanzen. 2010 veröffentlichte die Europäische Kommission erneut ein Kompendium, in dem sie die Ergebnisse von EU-finanzierten Studien durch über 400 unabhängige Arbeitsgruppen aus dem Zeitraum 2001-2010 zusammentrug. Seit über 25 Jahren Forschung gebe es keine Hinweise dafür, dass gentechnisch veränderte Pflanzen mit höheren Risiken für die menschliche Gesundheit verbunden seien als konventionelle.[72]
Laut einem Review von Domingo und Bordonaba (2011) hat die Zahl der veröffentlichten Sicherheitsuntersuchungen seit 2006 deutlich zugenommen. Mehrere zwischen Oktober 2006 und August 2010 erschienene Studien zu verschiedenen transgenen Maissorten hätten gezeigt, dass diese genauso sicher wie konventionelle Maissorten seien. Lediglich die Studien von Seralinis Gruppe im Bezug auf drei transgene Maissorten hätten Bedenken geäußert (siehe Abschnitt Kontroversen).[73]
Kontroversen
Eine Gruppe um den französischen Biologen Gilles-Eric Séralini veröffentlichte in der Vergangenheit mehrere Studien, die die durch Zulassungen sowie zahlreiche Studien attestierte gesundheitliche Unbedenklichkeit von mehreren transgenen Maissorten der Firma Monsanto (MON863, MON810, NK603) in Frage stellten.
Die Veröffentlichungen der Gruppe lösten heftige Kontrovesen aus. Mehrere Forschergruppen und Behörden untersuchten die Veröffentlichungen und warfen ihnen mangelnde Aussagekraft vor.
Seralinis Gruppe veröffentlicht seit Jahren Studien, welche spezifisch die Sicherheit von Monsantos Produkten in Frage stellen. Sie wird unter anderem von Greenpeace finanziert.[74] Seralini und seine Kollegen sind im Comité de Recherche et d’Information Indépendantes sur le Génie Génétique (CRIIGEN), welches die Auffassungen mehrerer europäischer und französischer Behörden bezüglich der Sicherheit von transgenem Mais ablehnt.[75]
Eine weitere Kontroverse entstand um ein Review von Dona und Arvanitoyannis (2009 in Critical Reviews in Food Science and Nutrition). Darin gehen die Autoren davon aus, dass viele Jahre weiterer Forschung notwendig seien, um die gesundheitlichen Auswirkungen zu erfassen. Die Resultate von Sicherheitsstudien zu transgenen Maissorten deuteten darauf hin, dass diese toxische (hepatische, renale, reprodukive) Effekte verursachen und hämatologische, biochemische und immunologische Parameter verändern können.[76] In derselben Fachzeitschrift behauptete Rickard (CropLife International) in einem Brief an den Herausgeber (2010), der Artikel von Dona und Arvanitoyannis enthalte viele unbelegte Behauptungen. Die Autoren zeigten, dass sie über das Grundwissen zur Sicherheitsbewertung von transgenen Pflanzen nicht verfügten und würden viele relevante wissenschaftliche Erkenntnisse entweder nicht kennen oder bewusst ignorieren.[77] Klaus Ammann warf Dona und Arvanitoyannis ebenfalls vor, ihre Zitierungen extrem gefiltert zu haben mit dem Ziel, ein negatives Bild von transgenen Pflanzen zu zeichnen. Ihr mangele es zudem an Kenntnissen auf dem Gebiet der Lebensmittelsicherheit. Zudem enthalte ihr Artikel viele Plagiate, die zudem aus Publikationen mit negativen Verzerrungen stammten, deren Inhalte vor kurzem oder vor längerem von anerkannten Wissenschaftlern in angesehenen Fachzeitschriften widerlegt worden seien.[78]
Seralini u. a. (2007)
Die Bt-Maissorte MON863 der Firma Monsanto enthält das Gen Cry3Bb1. Sie ist seit 2003 in den Vereinigten Staaten und Kanada für den Anbau und als Futter- und Lebensmittel zugelassen. Als Futter- und Lebensmittel ist MON863 unter anderem in Japan, Korea, Taiwan, den Philippinen, Australien und Neuseeland, China, Russland, Singapur, Mexiko and der EU zugelassen.[79]
Monsanto reichte den Zulassungantrag für MON863 als Futter- und Lebensmittel in der EU 2002 beim RKI ein. Das RKI überprüfte den Antrag und stellte auf Basis der von Monsanto durchgeführten 90-tägigen Fütterungsstudie (deren Dokumentation mehr als tausend Seiten umfasst und die später als Kurzfassung[80] veröffentlicht wurde) mit Ratten keine schädlichen Effekte von MON863 fest. Die EFSA stufte im April 2004 auf Basis derselben Studie MON863 als unbedenklich für Mensch, Tier und Umwelt ein. In der Fütterungsstudie wurden männliche und weibliche Ratten mit MON863 in verschiedenen Dosierungen oder mit der konventionellen Ausgangslinie sowie weiteren konventionellen Maissorten gefüttert. Sowohl beim Wachstum der Tiere als auch bei verschiedenen biologischen Parametern gab es vereinzelt statistisch signifikante Abweichungen bei den mit MON863 gefütterten Tieren, die von der EFSA als „biologisch nicht relevant“ bewertet wurden.[79][81][82]
In der Öffentlichkeit und unter französischen Wissenschaftlern der Commission du génie biomoléculaire (CGB) wurden Zweifel geäußert, ob die beobachteten Abweichungen bei den Ratten, die mit MON863 gefüttert wurden, im Rahmen der üblichen „biologischen Streuung“ liegen oder ob sie als Indizien für gesundheitliche Gefahren zu werten sind. Weitere Gutachten wurden eingeholt. Neue Gewebe-, Zell- und Organuntersuchungen ergaben kein anderes Bild. Der Verdacht, die erhöhte Zahl von weißen Blutkörperchen bei einigen MON863-Ratten sei ein Indiz für „echte Entzündung“, bestätigte sich nicht. Daraufhin schlossen sich auch die Experten der CGB der Sicherheitsbewertung der EFSA an. Greenpeace und andere Kritikergruppen forderten weiterhin die Herausgabe der vollständigen Fütterungsstudie, was Monsanto zunächst verweigerte. Das Oberverwaltungsgericht Münster bestimmte auf Antrag von Greenpeace, dass Monsanto die vollständigen Unterlagen aus dem Zulassungsverfahren offen legen muss. Auf einer Presskonferenz am 22. Juni 2004 in Berlin forderte Greenpeace die Bundesregierung auf, gegen eine Zulassung zu stimmen. Seralini sagte dort, angesichts der auffälligen Ergebnisse sei es notwendig, die Versuche zu wiederholen. Im Oktober 2004 bekräftigte das EFSA-Expertengremium, dass die Fütterungsstudien keine Hinweise auf gesundheitliche Bedenklichkeit lieferten. Die EU-Zulassung erfolgte als Futtermitel im August 2005, als Lebensmittel im Januar 2006.[81][82][83]
Im März 2007 veröffentlichte Seralinis Gruppe die von Greenpeace Deutschland finanziell unterstützte Studie „New Analysis of a Rat Feeding Study with a Genetically Modified Maize Reveals Signs of Hepatorenal Toxicity“ auf Basis einer Neubewertung von Monsantos Fütterungsdaten.[84][85] Seralini u. a. kamen darin zu dem Schluss, dass Ratten, die mit MON863-Maiskörner gefüttert wurden, geringfügige, aber dosierungsabhängige Abweichungen im Wachstum bei beiden Geschlechtern zeigten. Außerdem könnten einige der statistisch signifikanten Abweichungen etwa bei den Blut- und Urinmessungen als Hinweise auf Leber- oder Nierentoxizität gedeutet werden.[85]
Eine Arbeitsgruppe der EFSA untersuchte daraufhin die Analyse von Seralini, traf sich mit den Autoren und nahm selbst eine erneute Auswertung der Daten vor. Zusätzlich wurde ein französisches Institut mit einer weiteren Analyse der statistischen Auswertung der Daten beauftragt. Die zuständigen Behörden der Mitgliedstaaten wurden ebenfalls um eine Stellungnahme gebeten. Laut EFSA gab es mal geringere, mal höhere Werte, die als isolierte zufällige Phänomene gedeutet werden könnten. Unterschiede in Blut- und Urinwerten konnten nicht in Gewebeschnitten bestätigt werden, und weisen daher nicht auf Organschädigungen hin. Die Hypothese von Seralini u. a., die Unterschiede in der Gewichtszunahme basiere auf einer Störung des Hormonhaushalts könne nicht durch die experimentellen Daten belegt werden. Im Unterschied zu Seralini habe EFSA die biologische Relevanz aller statistisch signifikanten Unterschiede zwischen den mit gv-Mais gefütterten Tieren und der isogenen Kontroll-Gruppe eingeschätzt. Insgesamt gebe die Studie von Seralini u. a. keine neuen Hinweise auf toxikologische Effekte.[85]
Ein von Monsanto finanziell unterstütztes Expertengremium von 6 Wissenschaftlern aus den Vereinigten Staaten, Deutschland, Großbritannien und Kanada stellte kurz darauf fest, dass die von Seralini u. a. vorgebrachten Effekte sich nicht auf MON863 zurückführen ließen bzw. keinerlei Relevanz hätten, da Seralini u. a. weder eine Dosis-Wirkungs-Kurve, zeitliche Reproduzierbarkeit, eine Verbindung mit anderen Veränderungen (z.B. histopathologische), Effekte in beiden Geschlechtern, Unterschiede außerhalb der normalen Variation, noch einen biologisch plausiblen kausalen Mechanismus demonstrieren konnten.[86]
Die Geschäftsführerin der Kommission für Genetisch veränderte Lebens- und Futtermittel des BfR, Marianna Schauzu, hält die Unterschiede toxikologisch ebenfalls für nicht relevant. Die Unterschiede seien meist gering gewesen und lägen im Rahmen der historischen Kontrolldaten, die in früheren Studien mit Ratten desselben Stammes gewonnen wurden. Die Unterschiede zeigten keine Dosis-Abhängigkeit und sie seien nicht durch Unterschiede bei anderen Parametern, die auf einen Effekt im selben Organ hindeuten könnten, untermauert worden. Auch in den mikroskopischen Untersuchungen der Organe und Gewebe seien keine Effekte beobachtet worden, die auf eine toxikologische Relevanz der statistisch signifikanten Unterschiede bei den Laborparametern schließen ließen. Zudem hätten Untersuchungen der Zusammensetzung sowie des allergenen und toxikologischen Potenzials von MON863 keine Hinweise auf unbeabsichtigte Veränderungen ergeben.[87]
FSANZ, die in Australien und Neuseeland zuständige Zulassungsbehörde, begutachtete die ursprüngliche Fütterungsstudie 2005 und leitete daraus keine negativen Effekte durch MON863 ab. Die Veröffentlichung von Seralini u. a. würde laut einer unabhängig begutachteten Untersuchung durch FSANZ keine neuen Sicherheitsbedenken rechtfertigen. Alle statistischen Unterschiede zwischen den Fütterungsgruppen lägen innerhalb der normalen biologischen Variation. FSANZ verlangt keine Fütterungsstudien bei Zulassungsanträgen für gentechnisch verändere Lebensmittel, wenn die Pflanzen in ihrer Zusammensetzung zu konventionellen Pflanzen äquivalent sind (Substanzielle Äquivalenz). FSANZ hatte die von Monsanto im Rahmen des Zulassungsantrags in der EU durchgeführten 90-tägigen Fütterungsstudie an Ratten 2005 trotzdem evaluiert und keine Risiken aus ihr abgeleitet. FSANZ lagen zudem akute Toxizitätsuntersuchungen an Mäusen und eine Fütterungsstudie mit Hühnern vor, die alle keine Hinweise auf negative Effekte geliefert hätten.[88]
Vendomois u. a. (2009)
Im Dezember 2009 veröffentlichte Seralinis Gruppe erneut eine statistische Auswertung der Rohdaten von drei Fütterungsstudien mit MON863, MON810 und NK603.[89] Seralini u. a. sprechen aus verschiedenen Gründen den angestellten Fütterungsversuchen die statistische Aussagekraft ab und wollen bei ihrer eigenen Auswertung der Rohdaten zumindest Anzeichen für mögliche toxische Wirkungen erkannt haben.
Monsanto wies die Vorwürfe zurück und behauptete Vendomois u. a. verwänden ungeeignete statistische Methoden.[75] Laut EFSA sind die Schlussfolgerungen bezüglich möglicher Nieren- und Leberschäden durch die Maissorten nicht durch die in der Veröffentlichung präsentierten Daten gerechtfertigt. Mehrere der fundamentalen statischen Kritikpunkte an Seralini u. a. (2007) träfen bei Vendomois u. a. (2009) ebenfalls zu. Vendomois u. a. (2009) ermöglichten keinen toxikologischen Vergleich zwischen transgenen und konventionellen Sorten, da (1) die Resultate ausschließlich in Form von prozentualen Unterschieden in den einzelnen Variablen wiedergeben worden seien und nicht in den gemessenen Einheiten, (2) die berechneten Werte der getesteten toxikologischen Parameter in keinen Bezug zu der normalen Schwankungsbreite der Tierart gesetzt wurden, (3) die berechneten Werte der getesteten toxikologischen Paramter nicht mit der Variabilität von mit anderen Sorten gefütterten Tieren verglichen wurden, (4) die statistisch signifikanten Unterschiede keine Konsistenz über verschiedene Dosen aufweise, (5) die rein statistischen Argumente der Autoren nicht mit den Ergebnissen der drei Fütterungsstudien bezüglich Organpathologie, Histopathologie und Histochemie konsistent seien. Bezüglich des Vorwurfs von Vendemois u. a., die drei Fütterungsstudien seien nicht adäquat, sagte das EFSA, dass sie allesamt gemäß international definierter OECD-Standards durchgeführt worden.[90] In einem im März 2010 veröffentlichten wissenschaftlichen Gutachten zu einem Neuantrag von MON863 unter geänderten Richtlinien bekräftigte die EFSA ihre bisherigen Erkenntnisse zur Sicherheit von MON863. Für die neue Sicherheitsbewertung wurden weitere Daten beim Antragsteller angefordert. Diese wurden bei der Sicherheitsbewertung ebenso berücksichtigt wie eine Reihe neuer wissenschaftlicher Veröffentlichungen, inklusive Seralini u. a. (2007).[91][92]
Laut FSANZ bieten Vendomois u. a. keine plausible wissenschaftliche Erklärung für ihre Hypothese. Sie verzerrten die toxikologische Signifikanz ihrer Ergebnisse, indem sie außer statistischen keine biologischen Aspekte berücksichtigen würden, was keiner robusten toxikologischen Analyse entspreche. FSANZ geht davon aus, dass die berichteten Unterschiede vor allem zufällig aufgetreten seien und äußerte sich bezüglich der Sicherheit der zugelassenen Sorte MON863 zuversichtlich.[93]
Der französische Haut Conseil des biotechnologies urteilte, dass Vendomois u. a. (2009) ebenso wenig wie Seralini u. a. (2007) zulässige wissenschaftliche Elemente enthalte, die auf hämatologische, hepatische oder renale Toxzität der drei Maissorten hindeute. Die Publikation sei lediglich eine Liste von statistischen Unterschieden ohne den Versuch, sie biologisch oder toxikologisch zu interpretieren. Wie von vielen Behörden bereits wiederholt betont wurde, bewiesen signifikante statistische Unterschiede nicht die Existenz biologischer Störungen. Daher sei das auf diesen Unterschieden vorgebrachte Argument nicht zulässig. Zudem seien die Unterschiede meist bei nur einem Geschlecht, einem Zeitpunkt oder einer Dosis aufgetreten und es fehle zudem komplett der Bezug zu der Dauer der Exposition und der Stärke der Dosis. Zuletzt seien einige der zitierten Unterschiede das Gegenteil eines üblicherweise als solchen betrachteten Hinweises auf toxische Effekte.[94]
Umweltrisiken
Umweltorganisationen vertreten die Ansicht, dass beim Anbau von transgenem Mais verschiedene Umweltrisiken bestehen. Sie befürchten,
- dass neben den Zielinsekten auch weitere Organismen geschädigt werden können,
- dass ein Anbau von transgenem Mais in Mexiko durch Auskreuzungen auf wilde Artverwandte die Biodiversität verringern könnte.
Ein 2007 veröffentlichtes Review von wissenschaftlicher Literatur und Studien internationaler Organisationen aus 10 Jahren kam zu dem Schluss, dass keine wissenschaftlichen Beweise für Umweltschäden durch die bisher kommerzialisierten transgenen Pflanzen existierten.[95] Vor der Zulassung einer neuen transgenen Sorte zum Anbau sind umfangreiche Sicherheitsstudien erforderlich, die in der Regel mehrere Jahre dauern. Eine neue Sorte darf nur dann zugelassen werden, wenn eine Unbedenklichkeit für die Umwelt bestätigt wurde. Nach dem Beginn des kommerziellen Anbaus einer neuen Sorte ist in der EU zudem ein anbaubegleitendes Monitoring vorgesehen.[55]
Nichtzielorganismen
Das Bt-Toxin Cry1Ab ist für einige Arten der Gattung Schmetterlinge giftig. Anders als der Maiszünsler ernähren sich nur sehr wenige Schmetterlingsarten von Mais, könnten aber theoretisch indirekt über Bt-Maispollen geschädigt werden, die auf ihrer Nahrung landen. Eine 1999 veröffentlichte Laborstudie stellte eine Schädigung von Monarchfaltern fest, wenn sie mit Bt-Maispollen des Events 11 gefüttert wurden.[96] Daraus wurden in der Öffentlichkeit Befürchtungen abgeleitet, der Anbau von Bt-Mais könnte Populationen des Monarchfalters reduzieren. Wissenschaftler hingegen betonten, dass das Fütterungsexperiment diese Befürchtungen nicht rechtfertige. Weitere Laborexperimente fanden, dass Pollen des Events 176 Monarchfalterlarven schädigen, woraufhin das Event vom Markt genommen wurde. Feldstudien hingegen fanden keine Effekte auf Larven durch die verbreiteten Bt-Maisevents (MON810 und Bt 11), die 80mal weniger Toxin produzieren als Event 176. Feldstudien zeigten zudem, dass die in den Laborstudien verwendeten Pollenmengen unter Feldbedingungen unrealistisch hoch seien, und suggerierten, dass die Pollen von Event 11 möglicherweise mit anderen Pflanzenteilen vermischt wurde. Für die derzeit zugelassenen Events seien extrem hohe Pollendichten notwendig, um eine Schädigung von Larven zu erreichen. Zudem fanden Felduntersuchungen, dass nur ein geringer Anteil von 0,8 % der Monarchfalterpopulation Bt-Maispollen ausgesetzt sei. Die natürlich Mortalität von 80 % während der Larvenphase müsse zudem berücksichtigt werden, ebenso wie andere Faktoren, wie Verluste durch Habitatzerstörung, Einsatz von Insektiziden sowie Kollisionen mit Autos.[95] Eine 2010 veröffentlichte Simulation suggeriert, dass selbst unter pessimistischen Annahmen ein flächendeckender Anbau von Bt-Mais in Europa kaum negative Effekte auf Schmetterlingsarten hätte. In allen Regionen war die maximale errechnete Sterblichkeitsrate bei Tagpfauenauge und Admiral weniger als einer von 1572 Schmetterlingen, bei der Kohlmotte eine von 392. Im Mittel aller Regionen lag sie für Tagpfauenauge und Admiral bei einem von 5000, für die Kohlmotte bei einer auf 4367.[97]
Zudem wurden die Auswirkungen auf Nützlinge wie natürliche Feinde und Bestäuber untersucht. Bt-Mais gilt als unbedenklich für Honigbienen.[95][98] In Labor- und Gewächshausstudien waren natürliche Feinde wie Florfliegen lediglich dann negativ betroffen, wenn ihre Beute durch Bt-Toxine geschädigt wird. Feldstudien zeigten, dass natürliche Feinde aufgrund der geringeren Beuteverfügbarkeit in Bt-Feldern seltener vorhanden waren, diese Reduktion jedoch keine Auswirkungen auf die Population habe. Florfliegen und andere natürliche Feinde sind polyphag, und daher von der Reduktion bestimmter Beutearten nicht stark betroffen.[95] Zudem würden auch andere Instrumente der Schädlingsbekämpfung das Nahrungsangebot von natürlichen Feinden beeinflussen, und die meisten gegenwärtig genutzten Insektizide (vor allem Breitbandinsektizide wie Pyrethroide und Organophosphate) hätten stärkere negative Auswirkungen auf natürliche Feinde als Bt-Toxine. Zudem zeigen viele Untersuchungen, dass Unterschiede zwischen verschiedenen konventionellen Maissorten im Hinblick auf Effekte auf Nichtzielorganismen größer sind als die Unterschiede zwischen einer Bt-Maissorte und ihrer konventionellen Entsprechung.[99] Bei zahlreichen Untersuchungen konnten keine negativen Effekte von Bt-Pflanzen auf Bodenmakroorganismen (Fadenwürmer, Springschwänze, Landasseln, Milben und Regenwürmer) festgestellt werden.[95][100][101]
Biodiversität
In Mexiko ist der Anbau von transgenem Mais seit 1998 verboten, um Landrassen und wilde Verwandte vor möglichen Auskreuzungen zu schützen. Nach Zeitungsberichten widersetzen sich mexikanische Bauern jedoch diesem Verbot und bauen Bt-Mais an. 2001 veröffentlichte Nature eine kontroverse Studie, die über einen Fund von Transgenen in mexikanischen Mais-Landrassen berichtete. Nature zog die Veröffentlichung wenige Monate später zurück, da "die Datenlage die Veröffentlichung nicht rechtfertige".[102] Eine 2009 veröffentlichte Studie fand in 1% von über 100 untersuchten Feldern in Mexiko Bt-Gene in Mais-Landrassen. Dabei ist unklar, ob eine gentechnische Einbringung des Bt-Gens in Landrassen illegalerweise vorgenommen wurden, oder ob die Gene von regulären, illegal angebauten Bt-Maissorten unbeabsichtigt ausgekreuzt wurden.[103] Nach einer Verknappung des Maisangebots Anfang 2007 forderte der mexikanische Bauernverband die Zulassung von transgenem Mais für den Anbau.[104] Im Oktober 2009 wurden zwei Genehmigungen für den Versuchsanbau von transgenem Mais auf knapp 13 ha erteilt. Thema der Untersuchungen ist unter anderem die Frage, ob Mexiko mit transgenen Sorten seine Abhängigkeit von Importen verringern kann.[105] Fast 2000 Wissenschaftler protestierten in einer Petition gegen die Genehmigungen, da ihrer Ansicht nach Auskreuzungen auf Landrassen nicht verhindert werden können.[106] Die Zulassungsbehörden hingegen betonen, dass ein Abstand von 500m zu konventionellen Feldern eingehalten wird. Zudem soll die Aussaat zu unterschiedlichen Zeitpunkten stattfinden, und umliegende Bauern bezüglich möglicher Auskreuzung befragt werden.[106] Es gibt bisher keine wissenschaftlichen Hinweise dafür, dass eine mögliche Auskreuzung von Transgenen die Biodiversität des Mais verringern könnte. Der Genfluss, der Austausch von Genen zwischen Kultur- und Wildsorten, ist ein natürlicher Vorgang. Ob sich Gene aus konventionellen Hochleistungssorten oder transgenen Sorten in Landsorten dauerhaft etablieren und dadurch die Biodiversität verringern, hängt letztlich davon ab, ob sie den Nachkommen einen Selektionsvorteil verleihen. Laut dem internationalen Mais- und Weizenforschungsinstitut nimmt die Vielzahl der Maisrassen in Mexiko allein durch Einkreuzungen aus Kultursorten nicht ab.[107]
Weblinks
Einzelnachweise
- ↑ a b c d e Brookes, G. & Barfoot, P. (2006): Global impact of biotech crops: Socio-economic and environmental effects in the first ten years of commercial use. AgBioForum, 9(3), 139-151. [1] (englisch)
- ↑ Bundesamt für Verbraucherschutz und Lebensmittelsicherheit: Zugelassene Pflanzenschutzmittel
- ↑ a b Bravo A, Gill S, Soberón M (2007). „Mode of action of Bacillus thuringiensis Cry and Cyt toxins and their potential for insect control“. Toxicon 49 (4): 423-35. doi:10.1016/j.toxicon.2006.11.022. PMID 17198720
- ↑ a b USA: Anbau gv-Pflanzen 2009
- ↑ Verbot von Genmais Monsanto scheitert erneut vor Gericht Süddeutsche Zeitung, 28. Mai 2009. Abgerufen am 23. Oktober 2011
- ↑ Rita Batista & Maria Margarida Oliveira: Facts and fiction of genetically engineered food. Trends in Biotechnology Band 27(5): 277-286.
- ↑ Der Mais, der nur als Futtermittel zugelassen war. Transgen.de, 5. Dezember 2002.
- ↑ Monsanto und BASF legen Entdeckung eines Gens offen, das Mais vor Trockenheit schützt
- ↑ China gibt grünes Licht für den Anbau von gentechnisch verändertem Reis und Mais. Transgen, 28. November 2009.
- ↑ KJ Kramer, TD Morgan, JE Throne, FE Dowell, M Bailey, JA Howard: Transgenic avidin maize is resistant to storage insect pests. Nature Biotechnology 18(6), 2000; S. 670-674. PMID 10835608.
- ↑ a b William J. Thieman, Michael A. Palladino: Biotechnologie. Pearson Studium, München 2007. S. 195, ISBN 978-3-8273-7236-9.
- ↑ YC Zhu, JJ Jr Adamczyk, S West S.: Avidin, a potential biopesticide and synergist to Bacillus thuringiensis toxins against field crop insects.. Journal of Economic Entomology 98(5), 2005; S. 1566–1571. PMID 16334325.
- ↑ Christeller, J., Markwick, N., Burgess, E., Malone, L. (2010): The Use of Biotin-Binding Proteins for Insect Control. Journal of Economic Entomology. Vol. 103, Nr. 2, S. 497.508.
- ↑ JA Gathouse: Biotechnological Prospects for Engineering Insect-Resistant Plants. Plant Physiology 146, S. 881-887, 2008. PMID 18316644
- ↑ Der Treibstoff-Mais
- ↑ USDA approves Corn Amylase Trait for Enogen (englisch)
- ↑ Insect Resistance Management Fact Sheet for Bacillus thuringiensis (Bt) Corn Products
- ↑ a b James, C. (2010): Global Status of Commercialized Biotech/GM Crops: 2009. ISAAA Brief No. 41. ISAAA: Ithaca, NY.
- ↑ Statistische Ämter des Bundes und der Länder: Flächennutzung
- ↑ FAO (2010): FAOSTAT. FAO, Rome.
- ↑ a b c d e f Mais. Übersicht von Transgen.de, 29. Juli 2011.
- ↑ Zulassungspraxis in der EU
- ↑ Ergebnisse von bundesweitem GVO-Saatgut-Monitoring liegen vor
- ↑ "Illegaler Gen-Mais" ausgesät. Transgen.de, 6. Juni 2010.
- ↑ Aigner verbietet Anbau von „Genmais“ Süddeutsche Zeitung vom 14. April 2009
- ↑ Anbauverbot gentechnisch veränderten Mais in Österreich und Ungarn bleibt. Transgen.de, 2. März 2009.
- ↑ www.bvl.bund.de: Bescheid des Bundesamt für Verbraucherschutz und Lebensmittelsicherheit, Az 6788-02-13 (C/F/95/12-02), 17. April 2009
- ↑ Pressemitteilung des BMEVL vom 14. April 2009
- ↑ Gemeinsame Erklärung der Wissenschaftsorganisationen zur Grünen Gentechnik
- ↑ Verbot von Genmais Monsanto scheitert erneut vor Gericht Süddeutsche Zeitung, 28. Mai 2009. Abgerufen am 21. Oktober 2011
- ↑ www.bvl.bund.de: Stellungnahme der ZKBS zur Risikobewertung von MON810 – Neue Studien zur Umweltwirkung von MON810, Az. 6788-02-13, 7. Juli 2009
- ↑ Keine neuen Hinweise auf Umweltrisiken durch Gentechnik-Mais MON810
- ↑ Agnès Ricroch, Jean Baptiste Bergé, Marcel Kuntz (2009): Is the German suspension of MON810 maize cultivation scientifically justified? Transgenic Reserach, Vol. 19, Nr. 1, S. 1-12.
- ↑ biosicherheit.de: Französische Forscher kritisieren MON810-Verbot
- ↑ Der Gerichtshof äußert sich zu den Voraussetzungen, unter denen die französischen Behörden den Anbau der Maissorte MON 810 vorübergehend verbieten durften. Gerichtshof der Europäischen Union, Pressemittelung Nr. 86/11.
- ↑ Europäische Regelungen zur Gentechnikkennzeichnung von Lebensmitteln
- ↑ Bayerischer Verwaltungsgerichtshof: Beschluss vom 21. Juni 2007 (Aktenzeichen: 22 CE 07.1294)
- ↑ Gen-Mais: Eine Gefahr für Bienen und Honig?
- ↑ Honig mit Pollen aus gentechnisch veränderten Pflanzen: Zulassung erforderlich. Transgen.de, 6. September 2011.
- ↑ Honig und Nahrungsergänzungsmittel, die den Pollen eines GVO enthalten, sind aus GVO hergestellte Lebensmittel, die nicht ohne vorherige Zulassung in den Verkehr gebracht werden dürfen. Pressemitteilung 79/11. Urteil in der Rechtssache C-442/09 Karl Heinz Bablok u. a. / Freistaat Bayern. EuGH, 6. September 2011.
- ↑ Urteil: Honig mit gv-Pollen braucht Zulassung. Biotechnologie.de, 7. September 2011.
- ↑ Lebensmitteldatenbank: Honig. Transgen.de, 8. September 2011.
- ↑ Zum Anbau gentechnisch veränderten Maises in einem Naturschutzgebiet. Naturschutzrecht.
- ↑ a b Brookes, G., & Barfoot, P. (2010). Global impact of biotech crops: Environmental effects, 1996-2008. AgBioForum, 13(1), 76-94.
- ↑ Zusammenfassung der Studie Ökologische Effekte von gentechnisch verändertem Mais mit Insektenresistenz und/oder Herbizidresistenz
- ↑ Originalstudie
- ↑ Focus on yield - Biotech crops; evidence, outcomes and impacts 1996-2006 (englisch)
- ↑ Gemeinsame Forschungsstelle der EU: Adoption and impact of the first GM crop introduced in EU agriculture: Bt maize in Spain (englisch)
- ↑ National Research Council (2010): The Impact of Genetically Engineered Crops on Farm Sustainability in the United States. Washington, D.C.: The National Academies Press.
- ↑ W. D. Hutchison, E. C. Burkness, P. D. Mitchell, R. D. Moon, T. W. Leslie, S. J. Fleischer, M. Abrahamson, K. L. Hamilton, K. L. Steffey, M. E. Gray, R. L. Hellmich, L. V. Kaster, T. E. Hunt, R. J. Wright, K. Pecinovsky, T. L. Rabaey, B. R. Flood, E. S. Raun, (2010): Areawide Suppression of European Corn Borer with Bt Maize Reaps Savings to Non-Bt Maize Growers. Science, 8. Oktober 2010.
- ↑ Bt-Mais: Weniger Schädlingsfraß, weniger Mykotoxine
- ↑ Fungal Growth and Fusarium Mycotoxin Content in Isogenic Traditional Maize and Genetically Modified Maize Grown in France and Spain (englisch)
- ↑ [http://www.umweltbundesamt.at/fileadmin/site/publikationen/M144.pdf österreichisches Umweltbundesamt: HANDBUCH ZU MONITORING UND RESISTENZMANAGEMENT FÜR BT-MAIS]
- ↑ Doce años de estudios por parte del MARM confirman que el maíz transgénico Bt no tiene efectos negativos sobre el medio ambiente (spanisch)
- ↑ a b Bt-Mais: Sicher für Mensch und Umwelt? Biosicherheit.de 14. Mai 2008
- ↑ Bruce E. Tabashnik, J.B.J. van Rensburg, Yves Carriere (2009):Field-Evolved Insect Resistance to Bt Crops: Definition, Theory, and Data. Journal of Economic Entomology 102(6): 2011-2025.
- ↑ Aaron J. Gassmann, Jennifer L. Petzold-Maxwell u.a.: Field-Evolved Resistance to Bt Maize by Western Corn Rootworm. In: PLoS ONE. 6, 2011, S. e22629, doi:10.1371/journal.pone.0022629.
- ↑ Sicherheitsbewertung genetisch veränderter Lebens- und Futtermittel. Bundesinstitut für Risikobewertung, 2010.
- ↑ Suzie Key, Julian K-C Ma, Pascal M. W. Drake: Genetically modified plants and human health. In: Journal of the Royal Society of Medicine. Band 101, Nummer 6, 2008, S. 290–298, DOI:10.1258/jrsm.2008.070372.
- ↑ Committee on Identifying and Assessing Unintended Effects of Genetically Engineered Foods on Human Health (2004): Safety of Genetically Engineered Foods: Approaches to Assessing Unintended Health Effects. Institute of Medicine & National Research Council. The National Academies Press, ISBN 0-309-09209-4. S. 8.
- ↑ British Medical Association (2004): Genetically modified foods and health: a second interim statement.
- ↑ Gibt es Risiken für den Verbraucher beim Verzehr von Nahrungsprodukten aus gentechnisch veränderten Pflanzen? Union der deutschen Akademien der Wissenschaften.
- ↑ A. önig, A. Cockburn, R.W.R. Crevel, E. Debruyne, R. Grafstroem, U. Hammerling, I. Kimber, I. Knudsen, H.A. Kuiper, A.A.C.M. Peijnenburg, A.H. Penninks, M. Poulsen, M. Schauzu, J.M. Wal (2004): Assessment of the safety of foods derived from genetically modified (GM) crops. Food and Chemical Toxicology 42: 1047–1088.
- ↑ Aumaitre, A. (2004): Safety assessment and feeding value for pigs, poultry and ruminant animals of pest protected (Bt) plants and herbicide tolerant (glyphosate, glufosinate) plants: interpretation of experimental results observed worldwide on GM plants. Italian Journal of Animal Science 3: 107-121. Direkter Link zum pdf: [www.aspajournal.it/index.php/ijas/article/download/ijas.2004.107/185]
- ↑ Gerhard Flachowsky, Andrew Chesson, Karen Aulrich (2005): Animal nutrition with feeds from genetically modified plants. Archives of Animal Nutrition 59: 1–40.
- ↑ WHO (2005): Modern food biotechnology, human health and development: an evidence-based study. S. iii.
- ↑ Domingo, J. (2007): Toxicity Studies of Genetically Modified Plants: A Review of the Published Literature. Critical Reviews in Food Science and Nutrition 47: 721–733.
- ↑ GMO Panel: Safety and nutritional assessment of GM plants and derived food and feed: The role of animal feeding trials. Food and Chemical Toxicology 46: S2–S70.
- ↑ Maddalena Querci, Gijs Kleter, Jean-Paul Malingreau, Hermann Broll, Guy Van den Eede (2008): Scientific and technical contribution to the development of an overall health strategy in the area of GMOs. JRC Reference Reports. European Communities.
- ↑ Peggy G. Lemaux (2008): Genetically Engineered Plants and Foods: A Scientist's Analysis of the Issues (Part I). Annual Review of Plant Biology 59: 771-812.
- ↑ Javier A Magaña-Gómez & Ana M Calderón de la Barca (2009): Risk assessment of genetically modified crops for nutrition and health. Nutrition Reviews 67: 1–16.
- ↑ Europäische Kommission (2010): A decade of EU-funded GMO research (2001-2010).
- ↑ José L. Domingo & Jordi Giné Bordonaba (2011): A literature review on the safety assessment of genetically modified plants. Environment International 37: 734–742.
- ↑ Strong Suspicions of Toxicity in One GMO Corn (englisch)
- ↑ a b Monsanto Response: de Vendomois et al. 2009.
- ↑ Artemis Dona & Ioannis S. Arvanitoyannis (2009): Health Risks of Genetically Modified Foods. Critical Reviews in Food Science and Nutrition 49: 164–175.
- ↑ Craig Rickard (2009): Letter to the Editor. Critical Reviews in Food Science and Nutrition 50: 85-91.
- ↑ Klaus Ammann: Do GM crops pose a health risk to humans?
- ↑ a b Technical And Safety Information. Focus on MON 863 / YieldGard Rootworm. Monsanto.com
- ↑ B. Hammond, J. Lemen, R. Dudek, D. Ward, C. Jiang, M. Nemeth, J. Burns (2006): Results of a 90-day safety assurance study with rats fed grain from corn rootworm-protected corn. Food and Chemical Toxicology 44: 147–160
- ↑ a b MON863. Transgen.de, 13. Januar 2006.
- ↑ a b EFSA bleibt dabei: Keine Bedenken bei gv-Mais MON863. Biosicherheit.de, 28. Juni 2007.
- ↑ Keine Geheimnisse in Sicherheitsfragen. Biosicherheit.de, 24. Juni 2006.
- ↑ Gilles-Eric Seralini, Dominique Cellier, Joel Spiroux de Vendomois (2007): New Analysis of a Rat Feeding Study with a Genetically Modified Maize Reveals Signs of Hepatorenal Toxicity. Archives of Environmenatl Contamination and Toxicology 52: 596–602.
- ↑ a b c EFSA bleibt dabei: Keine Bedenken bei gv-Mais MON863. Transgen.de, 28. Juni 2007.
- ↑ J. Doull, D. Gaylor, H.A. Greim, D.P. Lovell, B. Lynch, I.C. Munro (2007): Report of an Expert Panel on the reanalysis by Séralini et al. (2007) of a 90-day study conducted by Monsanto in support of the safety of a genetically modified corn variety (MON 863). Food and Chemical Toxicology, Vol. 45, Nr. 11, S. 2073-2085.
- ↑ "Statistisch signifikante Unterschiede treten in praktisch allen Fütterungsstudien auf". BioSicherheit.
- ↑ FSANZ reaffirms its risk assessment of genetically modified corn MON 863. FSANZ, 25 Juli 2007.
- ↑ Joël Spiroux de Vendômois, François Roullier, Dominique Cellier, Gilles-Eric Séralini (2009): A Comparison of the Effects of Three GM Corn Varieties on Mammalian Health. International Journal of Biological Sciences 5: 706-726.
- ↑ Minutes of the 55th Plenary Meeting of the Scientific Panel on Genetically Modified Organisms held on 27-28 January 2010 in Parma, Italy.
- ↑ EFSA-Gutachten: Erneut keine Sicherheitsbedenken bei Gentechnik-Mais MON863. Transgen.de, 7. April 2010.
- ↑ EFSA Panel on Genetically Modified Organisms (2010): Scientific Opinion on an application (EFSA-GMO-RX-MON863) for renewal of the authorisation for continued marketing of existing feed materials, feed additives and food additives produced from maize MON863, under Regulation (EC) No 1829/2003 from Monsanto. EFSA Journal 8: 1562.
- ↑ FSANZ response to de Vendomois et al. (2009). Food Standards Australia New Zealand, 2009. (englisch)
- ↑ Opinion relating to the deposition of 15 December 2009 by the Member of Parliament, François Grosdidier, as to the conclusions of the study entitled “A comparison of the effects of three GM corn varieties on mammalian health” by J. Spiroux de Vendômois, F. Roullier, D. Cellier and G.E. Séralini, Int. J. Biol. Sci, 2009: 5(7) : 706-726. High Council of Biotechnologies. Scientific Committee, 2009 (Übersetzung der Food Standards Agency).
- ↑ a b c d e Sanvido O., Romeis J., Bigler F.(2007): Ecological impacts of genetically modified crops: ten years of field research and commercial cultivation. Advances in biochemical engineering/biotechnology. Vol 107, pp. 235-78.
- ↑ Losey, J., Rayor, L., Carter, M. (1999): Transgenic pollen harms monarch larvae. Nature, Vol. 399, S. 214.
- ↑ Selbst bei flächendeckendem Anbau von Bt-Mais kaum Gefährdung für Schmetterlinge. Biosicherheit.de, 7. Juni 2010.
- ↑ Biosicherheit.de – Honigbiene
- ↑ Agnès Ricroch, Jean Baptiste Bergé, Marcel Kuntz (2009): Is the German suspension of MON810 maize cultivation scientifically justified? Transgenic Reserach, Vol. 19, Nr. 1, S. 1-12.
- ↑ Langzeit-Studie: Anbau von Bt-Mais ohne Einfluss auf Regenwürmer. Biosicherheit.de, 18. Mai 2010.
- ↑ FAL-Daten zeigen keine Gefahr von Gen-Mais für Bodenmikroorganismen
- ↑ Transgenic DNA discovered in native Mexican corn, according to a new study by UC Berkeley researchers. Press Release, 29. November 2001, UC Berkeley.
- ↑ Dalton, R. (2008): Modified genes spread to local maize. Nature, Vol. 456, published online 12 November 2008.
- ↑ Mexiko: Spuren von gentechnisch verändertem Mais bestätigt. Biosicherheit, 11. März 2009
- ↑ Mexico issues first permits to grow GM corn (englisch)
- ↑ a b Mexico's transgenic maize under fire. Nature, Vol. 462, Nr. 404, 2009.
- ↑ Fremdgene in Landsorten: Gefahr für die biologische Vielfalt? 10.Februar 2003.
Wikimedia Foundation.