- Thallium(I)-chlorat
-
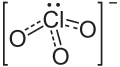
Strukturformel 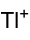
Allgemeines Name Thallium(I)-chlorat Andere Namen Thalliumchlorat
Summenformel TlClO3 CAS-Nummer 13453-30-0 PubChem 61610 Kurzbeschreibung Feststoff[1]
Eigenschaften Molare Masse 287,82 g·mol−1 Aggregatzustand fest
Löslichkeit leicht löslich in Wasser[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [2] 


Gefahr
H- und P-Sätze H: 330-300-373-411 EUH: keine EUH-Sätze P: ? EU-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [2] 

Sehr giftig Umwelt-
gefährlich(T+) (N) R- und S-Sätze R: 26/28-33-51/53 S: (1/2)-13-28-45-61 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Thallium(I)-chlorat ist eine chemische Verbindung aus der Gruppe der Thalliumverbindungen und Chlorate.
Gewinnung und Darstellung
Thallium(I)-chlorat kann durch Reaktion von Thallium(I)-sulfat mit Bariumchlorat hergestellt werden.
Eigenschaften
Thallium(I)-chlorat ist ein Feststoff, welcher leicht löslich in Wasser ist.[1] Er zersetzt sich bei Erhitzung, wobei Chlorverbindungen und Thalliumverbindungen (Thallium(III)-oxid und Thallium(I)-chlorid) entstehen.[3]
Thallium(I)-chlorat ist ein starkes Oxidationsmittel und muss wie alle Chlorate vorsichtig gehandhabt werden.
Einzelnachweise
- ↑ a b c Eintrag zu CAS-Nr. 13453-30-0 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 22. Dezember 2010 (JavaScript erforderlich)
- ↑ a b Nicht explizit in EU-Verordnung (EG) 1272/2008 (CLP) gelistet, fällt aber dort mit der angegebenen Kennzeichnung unter den Sammelbegriff „Thalliumverbindungen“; Eintrag in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. März 2009 (JavaScript erforderlich)
- ↑ Andrew Knox Galwey and Michael E. Brown; Thermal decomposition of ionic solids, S. 371; ISBN 978-0444824370
Kategorien:- Giftiger Stoff
- Umweltgefährlicher Stoff
- Thalliumverbindung
- Chlorat
Wikimedia Foundation.

