- Bariumperoxid
-
Kristallstruktur 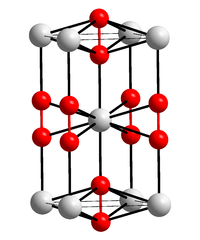
__ Ba2+ __ O- Allgemeines Name Bariumperoxid Andere Namen Bariumsuperoxid
Verhältnisformel BaO2 CAS-Nummer - 1304-29-6
- 12230-86-3 (Oktahydrat)
Kurzbeschreibung farbloser Feststoff[1]
Eigenschaften Molare Masse 169,34 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Siedepunkt Zersetzung bei 800 °C[2]
Löslichkeit - gering in Wasser (Zersetzung)[2]
- unlöslich in Ethanol und Diethylether[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [4] 

Gefahr
H- und P-Sätze H: 272-332-302 EUH: keine EUH-Sätze P: 220 [5] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [4] 

Brand-
förderndGesundheits-
schädlich(O) (Xn) R- und S-Sätze R: 8-20/22 S: (2)-13-27 MAK 0,5 g·m−3 (Barium)[6]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Bariumperoxid ist eine chemische Verbindung der Elemente Barium und Sauerstoff mit der Summenformel BaO2. Beim Erhitzen über 700 °C gibt BaO2 Sauerstoff ab. Bariumperoxid kann aufgrund seiner Verwandtschaft zum H2O2 als Oxidations- wie auch als Reduktionsmittel wirken.
Inhaltsverzeichnis
Geschichte
Bariumperoxid ist die erste durch Alexander von Humboldt (1799) bekannt gewordene Peroxo-Verbindung.[7]
Herstellung
Hergestellt wird Bariumperoxid, indem Bariumoxid unter erhöhtem Druck mit Luft auf etwa 500 °C erhitzt wird.
Im Labor kann es auch aus Bariumchloridlösung und Wasserstoffperoxid im Basischen gewonnen werden. Dabei entsteht zunächst das Oktahydrat, das anschließend durch Erhitzen in Bariumperoxid umgewandelt werden kann.Eigenschaften
Bariumperoxid ist ein sehr reaktionsfähiger brandfördernder weißer bis grauer Feststoff, welcher sich in Wasser zersetzt. Er zersetzt sich ab einer Temperatur von 700 °C, wobei Sauerstoff und Bariumoxid entsteht.[8] Bariumperoxid besitzt eine tetragonale Kristallstruktur mit der Raumgruppe I4/mmm, während das Oktahydrat ebenfalls eine tetragonale Kristallstruktur jedoch mit der Raumgruppe P4/mcc besitzt.[3]
Verwendung
Bariumperoxid wird hauptsächlich in der Pyrotechnik als Sauerstofflieferant und zur Erzeugung von grünen Flammenfärbungen verwendet. Mit Magnesiumpulver findet es in Zündkirschen Anwendung. Auch dient es zum Entfärben von Bleigläsern und zum Bleichen von Stroh und Seide.
Früher spielte Bariumperoxid zur großtechnischen Herstellung von Wasserstoffperoxid (so genanntes Brinsches Peroxid-Verfahren) eine große Rolle:
Erläuterung:
- Umwandlung des Sulfats in das Oxid, das SO2 wird zur Herstellung der im dritten Schritt benötigten Schwefelsäure eingesetzt.
- Synthese des Bariumperoxids
- Gewinnung des Wasserstoffperoxids; das BaSO4 wird als Rohstoff in den Kreislauf zurückgegeben
Heutzutage ist dieses Vorgehen praktisch vollständig vom energetisch weniger aufwändigen Anthrachinon-Verfahren verdrängt.
Sicherheitshinweise
Beim Mischen von Bariumperoxid mit brennbaren Stoffen besteht Explosionsgefahr.[8]
Einzelnachweise
- ↑ a b Helmut Sitzmann, in: Roempp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c d Datenblatt Bariumperoxid bei Merck, abgerufen am 19. Januar 2011.
- ↑ a b Jean D'Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-5406-0035-0, S. 328 (Eingeschränkte Vorschau in der Google Buchsuche).
- ↑ a b Eintrag zu CAS-Nr. 1304-29-6 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Datenblatt Bariumperoxid bei Sigma-Aldrich, abgerufen am 9. März 2011.
- ↑ Datenblatt Bariumperoxid bei AlfaAesar, abgerufen am 9. Februar 2010 (JavaScript erforderlich).
- ↑ Winnacker Küchler, Chemische Technololgie Band 1, 3. Auflage 1970, Seite 514
- ↑ a b Eintrag zu CAS-Nr. 1304-29-6 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 22. Mai 2011 (JavaScript erforderlich).
Literatur
- Römpp Chemie-Lexikon, 9. Auflage. Thieme-Verlag.
Kategorien:- Gesundheitsschädlicher Stoff
- Brandfördernder Stoff
- Peroxid
- Bariumverbindung
Wikimedia Foundation.




