- Katalysator
-
Katalysator (von der Katalyse, griechisch, katálysis – Auflösung mit lateinischer Endung) bezeichnet in der Chemie einen Stoff, der die Reaktionsgeschwindigkeit durch die Senkung der Aktivierungsenergie einer chemischen Reaktion erhöht, ohne dabei selbst verbraucht zu werden. Er beschleunigt die Hin- und Rückreaktion gleichermaßen und ändert somit die Kinetik chemischer Reaktionen, nicht deren Thermodynamik .
Ein Katalysator nimmt an einer chemischen Reaktion unter Bildung einer intermediären Stufe mit den Reaktanden teil, aus dem der Katalysator nach Entstehung des Produkts unverändert freigesetzt wird. Ein Katalysator kann diesen so genannten Katalysezyklus viele Male durchlaufen.
Je nachdem in welchen Phase Katalysator und Edukte vorliegen, spricht man von homogenen oder heterogenen Katalysatoren. Biochemische Prozesse werden durch Enzyme katalysiert.
Inhaltsverzeichnis
Geschichte
Vermutlich waren es die Assyrer vor über 5000 Jahren, die katalytische Prozesse erstmals bei der Gärung von Alkohol einsetzten. Seit der Antike werden chemische Reaktionen mit Hilfe von Katalysatoren ausgeführt. Erst Jöns Jakob Berzelius kam 1835 zu der Erkenntnis, dass eine Vielzahl von Reaktionen nur dann erfolgte, wenn ein bestimmter Stoff zugegen war, der jedoch nicht verbraucht wurde. Seiner Meinung nach wurden diese Stoffe nicht umgesetzt, lieferten jedoch durch ihre Anwesenheit die Energie über ihre katalytische Kraft. Er bezeichnete diese Stoffe als Katalysatoren.
In der Folgezeit gelang es, tieferes Verständnis für die thermodynamischen Hintergründe der Katalyse zu gewinnen. Wilhelm Ostwald definierte den Katalysator 1895 wie folgt:
„Ein Katalysator ist ein Stoff, der die Geschwindigkeit einer chemischen Reaktion erhöht, ohne selbst dabei verbraucht zu werden und ohne die endgültige Lage des thermodynamischen Gleichgewichts dieser Reaktion zu verändern“
– Wilhelm Ostwald: [1].
Für seine Arbeiten um die Katalyse erhielt Wilhelm Ostwald den Nobelpreis für Chemie.
Chemie
Die Wirkungsweise eines Katalysators beruht auf seiner Möglichkeit, den Mechanismus einer chemischen Reaktion derart zu verändern, dass die Aktivierungsenergie verändert wird. Man „geht einen anderen Weg“ auf der Potential-Hyperebene.
Das Potential ist im Allgemeinen eine Funktion mehrerer Variablen. Deshalb ist im einfachsten Fall, nämlich der Abhängigkeit des Potentials von nur zwei Variablen, die sich ändern, das Potential eine dreidimensionale Ebene. Die Variablen können z. B. zwei Bindungsabstände zwischen den Reaktanden sein, die sich während der Reaktion ändern. Dieser einfachste Fall ist zwar anschaulich, aber unrealistisch.
Dieses geschieht über die Bildung einer reaktiven Zwischenstufe und deren Abreaktion zu den Endprodukten, wobei der eingesetzte Katalysator zurückgebildet wird. In der Praxis werden allerdings Katalysatoren in der Regel durch Nebenreaktionen nach einiger Zeit des Gebrauchs unwirksam, da sie durch Nebenprodukte blockiert werden. Die folgende Grafik ergibt sich als Schnitt durch die Energie-Hyperpotentialfläche.
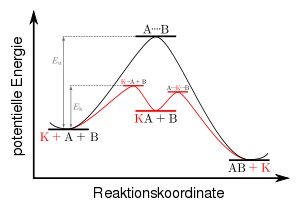
In der Grafik gibt die obere Kurve (schwarz) die nicht-katalysierte Reaktion
wieder. Die Aktivierungsenergie dieser unkatalysierten Reaktion wird mit Eu bezeichnet. Die untere Kurve (rot) zeigt den Energieverlauf der durch K katalysierten Reaktion an. Hier wird über einen Übergangszustand (erstes Profilmaximum) eine Zwischenstufe KA (lokales Profilminimum) erreicht:
Über einen weiteren Übergangszustand (zweites Profilmaximum) wird das Produkt AB gebildet, wobei der Katalysator K zurückgebildet wird:
Die mit Ek bezeichnete Aktivierungsenergie der katalysierten Reaktion ist geringer.
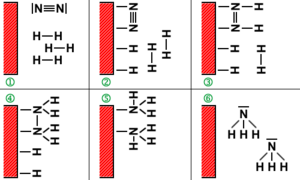
Als Beispiel kann die katalytische Verbrennung von Wasserstoff mit Sauerstoff angeführt werden. Diese Verbrennung ist thermodynamisch so günstig, dass sie prinzipiell „freiwillig“ ablaufen sollte, jedoch aufgrund der bei Zimmertemperatur hohen Aktivierungsenergie so stark gehemmt ist, dass die Reaktionsgeschwindigkeit sehr gering ist. Die Anwesenheit eines Platinkatalysators kann diese Aktivierungsenergie derart erniedrigen, dass diese Reaktion dann hinreichend schnell auch bei niedrigeren Temperaturen abläuft. Eine Anwendung dafür war das Döbereinersche Feuerzeug.
Bei Gleichgewichtsreaktionen verändert ein Katalysator Hin- und Rückreaktion auf die gleiche Weise, so dass die Lage des Gleichgewichts nicht verändert wird, das Gleichgewicht sich aber schneller einstellt.
Bedeutung der Katalysatoren
 Aufgeschnittener Fahrzeugkatalysator
Aufgeschnittener Fahrzeugkatalysator
Katalysatoren kommen in der Natur in vielfältiger Weise vor. In Lebewesen laufen fast alle lebensnotwendigen chemischen Reaktionen katalysiert ab (z. B. bei der Photosynthese, der Atmung oder der Energiegewinnung aus der Nahrung). Die verwendeten Katalysatoren sind meist bestimmte Eiweiße, die Enzyme.
Die Herabsetzung der Aktivierungsenergie durch Katalysatoren ist bei chemischen Reaktionen von großer kommerzieller Bedeutung. In mehr als 80 % aller chemischen industriellen Prozesse werden Katalysatoren eingesetzt. Ohne die Anwesenheit des Katalysators würde die jeweilige chemische Reaktion sehr viel langsamer oder gar nicht erfolgen. Deshalb sind Katalysatoren heutzutage kaum noch aus der Chemietechnik wegzudenken. Derzeit wird geschätzt, dass etwa 80 % aller chemischen Erzeugnisse eine katalytische Stufe in ihrer Wertschöpfungskette durchlaufen.
Entstehen bei Reaktionen mehrere Produkte, spielt die Selektivität eines Katalysators eine sehr wichtige Rolle. Dabei wird der Katalysator so gewählt, dass nur diejenige Reaktion beschleunigt wird, die das erwünschte Produkt erzielt. Verunreinigungen durch Nebenprodukte werden so weitgehend vermieden.
Aus der Sicht des Umweltschutzes wird durch den Einsatz von selektiven und aktiven Katalysatoren in der Regel Energie eingespart und die Menge an Nebenprodukten reduziert. Nicht minder bedeutsam für unsere Umwelt ist aber auch die Abgasnachbehandlung in der industriellen Produktion oder in Elektrizitätswerken. Im Falle der abgaskatalytischen Verfahren (z. B. in PKW) werden unvermeidbare, gefährliche Substanzen in weniger gefährliche umgesetzt.
Beispiel: Im Autoabgaskatalysator reagiert das Atemgift Kohlenstoffmonoxid (CO) sowie unverbrannte Kohlenwasserstoffe mit NOx und Sauerstoff (O2) zum ungiftigen Kohlenstoffdioxid (CO2) sowie Stickstoff und Wasser (H2O).
Beispiele für Katalysatoren
 links: Teilweise karamellisierter Würfelzucker, rechts: Verbrennung eines Zuckerwürfels mit Asche als Katalysator
links: Teilweise karamellisierter Würfelzucker, rechts: Verbrennung eines Zuckerwürfels mit Asche als Katalysator
Cereisen (Ammoniaksynthese), Raney-Nickel, Platin, Rhodium, Palladium, Braunstein, Vanadiumpentoxid und Samarium(III)-oxid katalysieren die Hydrierung und Dehydrierung von Ethanol.
Hopcalite, eine Gruppe von Katalysatoren aus verschiedenen Metalloxiden, katalysieren die Oxidation von Kohlenstoffmonoxid zu Kohlenstoffdioxid bei Raumtemperatur.
Fahrzeugkatalysator: Bekanntestes Beispiel ist der Katalysator im Automobil zur Reduktion der Abgasemissionen, bei dem das ganze Gerät nach dem chemisch-physikalischen Prinzip benannt ist.
Wichtige katalytische Verfahren
Verfahren Produkt Katalysator Bedingung Reaktor Haber-Bosch-Verfahren NH3 α-Eisen/Al2O3 T = 450…500 °C; p = 25…40 MPa Festbettreaktor Methanolherstellung CH3OH CuO/Cr2O3, ZnO/Cr2O3 oder CuO/ZnO T = 210…280 °C; p = 6 MPa Festbettreaktor Kontaktverfahren H2SO4 V2O5/Träger T = 400…500 °C Festbettreaktor Ostwaldverfahren HNO3 Platin/Rhodium T = 800 °C Literatur
- F. Schüth: Schlüsseltechnologie der chemischen Industrie: Heterogene Katalyse, in: Chemie in unserer Zeit 2006, 40, 92–103.
- M. Röper: Homogene Katalyse in der chemischen Industrie, in: Chemie in unserer Zeit 2006, 40, 126–135.
- R. Stürmer, M. Breuer: Enzyme als Katalysatoren. Chemie und Biologie Hand in Hand, in: Chemie in unserer Zeit 2006, 40, 104–111.
Siehe auch
Einzelnachweise
- ↑ Eugen Hintsches: Nanozwiebeln würzen die Styrolchemie. In: Materialwissenschaften, Nr. 4, 2002, S. 44–50 (PDF, S. 48)
Weblinks
-
 Commons: Catalysts – Sammlung von Bildern, Videos und Audiodateien
Commons: Catalysts – Sammlung von Bildern, Videos und Audiodateien -
 Wiktionary: Katalysator – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Katalysator – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wikimedia Foundation.